Foram encontradas 70 questões.
A respeito do sulfato de magnésio puro, julgue os próximos itens.
I O sulfato de magnésio é uma substância molecular.
II O sulfato de magnésio puro possui íons livres.
III A fusão do sulfato de magnésio ocorre com o desprendimento de energia.
Assinale a opção correta.
I O sulfato de magnésio é uma substância molecular.
II O sulfato de magnésio puro possui íons livres.
III A fusão do sulfato de magnésio ocorre com o desprendimento de energia.
Assinale a opção correta.
Provas
Questão presente nas seguintes provas
Em laboratórios de química e física, sistemas usados para
verificar se determinada solução é condutora de eletricidade ou
isolante podem ser construídos a partir de uma fonte de tensão
(multímetro), uma lâmpada LED, fios e béquer contendo uma
solução. Com a imersão dos fios na substância, o circuito elétrico
é completado.
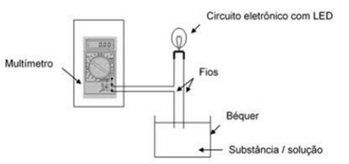
A partir dessas informações, julgue os itens a seguir.
I A lâmpada LED acenderá quando o béquer contiver íons livres em solução.
II Se o béquer contiver água desmineralizada, a lâmpada LED não acenderá.
III Se os fios forem de cobre, a lâmpada LED acenderá, independentemente da natureza da solução.
Assinale a opção correta.

A partir dessas informações, julgue os itens a seguir.
I A lâmpada LED acenderá quando o béquer contiver íons livres em solução.
II Se o béquer contiver água desmineralizada, a lâmpada LED não acenderá.
III Se os fios forem de cobre, a lâmpada LED acenderá, independentemente da natureza da solução.
Assinale a opção correta.
Provas
Questão presente nas seguintes provas
4,0 g de uma amostra de Zn, 80% puro, foi tratada com
0,05 mol de uma solução aquosa de HCl. As massas molares do
Zn, do H e do Cl são, respectivamente, iguais a 65,4 g/mol,
1,0 g/mol e 35,5 g/mol.
Zn(s) + HCl(aq) → ZnCl2(aq) + H2 (g)
Considerando as informações do texto precedente e a equação química da reação, não balanceada, apresentada anteriormente, assinale a opção correta.
Zn(s) + HCl(aq) → ZnCl2(aq) + H2 (g)
Considerando as informações do texto precedente e a equação química da reação, não balanceada, apresentada anteriormente, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Texto 12A2-III
Álcoois são compostos que contém o(s) grupo(s)
hidroxila(s) ligado(s) ao(s) átomo(s) de carbono(s) de hibridação
sp3
. São substâncias bastante comuns na natureza e têm grande
aplicação industrial e farmacêutica. O etanol, por exemplo, é
usado como solvente, como aditivo na gasolina e como bebida.
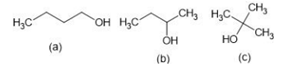
De acordo com o número de grupos orgânicos ligados ao carbono
que contém a hidroxila, os álcoois se classificam em primários,
secundários e terciários e essa classificação está associada às
suas propriedades físicas.
Provas
Questão presente nas seguintes provas
Texto 12A2-III
Álcoois são compostos que contém o(s) grupo(s)
hidroxila(s) ligado(s) ao(s) átomo(s) de carbono(s) de hibridação
sp3
. São substâncias bastante comuns na natureza e têm grande
aplicação industrial e farmacêutica. O etanol, por exemplo, é
usado como solvente, como aditivo na gasolina e como bebida.
De acordo com o número de grupos orgânicos ligados ao carbono
que contém a hidroxila, os álcoois se classificam em primários,
secundários e terciários e essa classificação está associada às
suas propriedades físicas.

Provas
Questão presente nas seguintes provas
Texto 12A2-II
No controle de qualidade de medicamentos contendo o
íon Fe2+, como o ferinsol, a concentração do íon ferroso pode ser
determinada por espectrofotometria, utilizando o complexo
formado entre Fe2+ e 1,10-fenantrolina, cuja absorbância é
medida em 480 nm. Para a análise, foram preparadas as soluções
a seguir.
i. cloridrato de hidroxilamina: 50 mL; 5%; fórmula molecular:
NH4ClO; MM = 69,5 g/mol
ii. acetato de sódio: 50 mL; 2M; fórmula molecular:
CH3COONa; MM = 82,0 g/mol
iii. 1,10-fenantrolina: 0,25%; fórmula molecular: C12H8N2; MM
= 180,3 g/mol
iv. sulfato ferroso amoniacal: 50 mL; 0,02 mg/mol de Fe2+;
fórmula molecular: FeH20N2O14S2; MM = 392,2 g/mol
Para traçar a curva padrão de Fe2+, foram preparados seis
balões volumétricos de 50 mL, nos quais foram adicionados
volumes crescentes da solução padrão de sulfato ferroso
amoniacal e volumes fixos das demais soluções reagentes
(cloridrato de hidroxilamina, acetato de sódio e
1,10-fenantrolina), completando-se o volume com água destilada.
O medicamento ferinsol foi diluído na proporção 1:1.000, e a
absorbância da solução diluída foi 0,450. A curva padrão obtida
apresentou a equação: y = 3,9509x − 0,0154, em que R2 = 0,9960.
Provas
Questão presente nas seguintes provas
Texto 12A2-II
No controle de qualidade de medicamentos contendo o
íon Fe2+, como o ferinsol, a concentração do íon ferroso pode ser
determinada por espectrofotometria, utilizando o complexo
formado entre Fe2+ e 1,10-fenantrolina, cuja absorbância é
medida em 480 nm. Para a análise, foram preparadas as soluções
a seguir.
i. cloridrato de hidroxilamina: 50 mL; 5%; fórmula molecular:
NH4ClO; MM = 69,5 g/mol
ii. acetato de sódio: 50 mL; 2M; fórmula molecular:
CH3COONa; MM = 82,0 g/mol
iii. 1,10-fenantrolina: 0,25%; fórmula molecular: C12H8N2; MM
= 180,3 g/mol
iv. sulfato ferroso amoniacal: 50 mL; 0,02 mg/mol de Fe2+;
fórmula molecular: FeH20N2O14S2; MM = 392,2 g/mol
Para traçar a curva padrão de Fe2+, foram preparados seis
balões volumétricos de 50 mL, nos quais foram adicionados
volumes crescentes da solução padrão de sulfato ferroso
amoniacal e volumes fixos das demais soluções reagentes
(cloridrato de hidroxilamina, acetato de sódio e
1,10-fenantrolina), completando-se o volume com água destilada.
O medicamento ferinsol foi diluído na proporção 1:1.000, e a
absorbância da solução diluída foi 0,450. A curva padrão obtida
apresentou a equação: y = 3,9509x − 0,0154, em que R2 = 0,9960.
Provas
Questão presente nas seguintes provas
Os haletos orgânicos são compostos pouco solúveis em água.
Apesar de o íon cloreto estar presente em grandes quantidades
nos sistemas vivos, até hoje poucos compostos halogenados
advindos do metabolismo dos animais superiores foram
estudados. Por outro lado, o íon iodeto é extraído do sangue e
concentrado na glândula tireoide, onde se forma o hormônio
tetraiodotironina (T4), cuja molécula é ilustrada pela figura a
seguir.
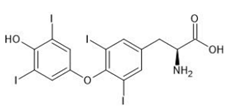
O T4 é uma substância liberada na corrente sanguínea pelas glândulas endócrinas e é o responsável pela regulação de uma variedade de funções fisiológicas.
A partir das informações precedentes, assinale a opção correta.

O T4 é uma substância liberada na corrente sanguínea pelas glândulas endócrinas e é o responsável pela regulação de uma variedade de funções fisiológicas.
A partir das informações precedentes, assinale a opção correta.
Provas
Questão presente nas seguintes provas
O tratamento adequado de resíduos em laboratórios de
análise de águas não é apenas uma prática ambientalmente
responsável, mas uma exigência fundamental para garantir o
controle de qualidade analítica. Além disso, esse processo está
diretamente alinhado aos requisitos da norma ISO 9001:2008,
que prioriza a gestão eficiente e o cumprimento de padrões de
qualidade.
A partir dessas informações, é correto afirmar que o conhecimento acerca do tratamento de resíduos contribui para assegurar a conformidade com os princípios da referida norma e a excelência nas análises realizadas, pois
A partir dessas informações, é correto afirmar que o conhecimento acerca do tratamento de resíduos contribui para assegurar a conformidade com os princípios da referida norma e a excelência nas análises realizadas, pois
Provas
Questão presente nas seguintes provas
O método ilustrado na figura a seguir descreve a extração de pesticidas em amostras de tomate, seguido por análise em cromatografia gasosa com detector por captura de elétrons (GC/ECD).
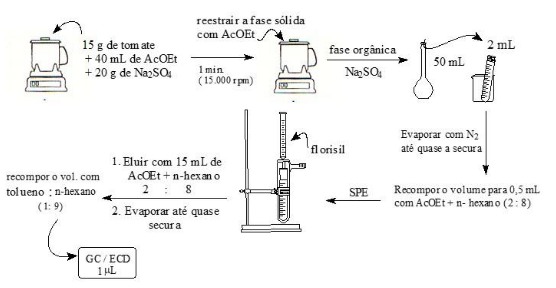
A tabela a seguir apresenta as concentrações das soluções mistas intermediárias dos pesticidas utilizadas para a quantificação.
| pesticida | sol. mista intermediária | sol. 1 | sol. 2 | sol. 3 | sol. 4 | sol. 5 |
|---|---|---|---|---|---|---|
| (ng/µl) | (pg/µl) | (pg/µl) | (pg/µl) | (pg/µl) | (pg/µl) | |
| quintozene | 2,5 | 12,5 | 25,0 | 50,0 | 75,0 | 125 |
| clorotalonil | 6,0 | 30,0 | 60,0 | 120 | 180 | 300 |
| iprodiona | 24,0 | 120 | 240 | 480 | 720 | 1.200 |
| fenpropatrin | 9,5 | 47,5 | 95,0 | 190 | 285 | 475 |
| β-ciflutrina | 10,5 | 52,5 | 105 | 210 | 315 | 525 |
| α-cipermetrina | 14,0 | 70,0 | 140 | 280 | 420 | 700 |
| fenvalerato | 15,5 | 77,5 | 155 | 310 | 465 | 775 |
| deltametrina | 20,0 | 100 | 200 | 400 | 600 | 1.000 |
M. H. Conceição. Tese de Doutorado. Instituto de Química, Universidade de Brasília, 2002.
A partir das informações precedentes, assinale a opção correta acerca do procedimento descrito.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container