Foram encontradas 51 questões.
Para caracterizar uma água, são determinados diversos parâmetros, os quais representam as suas características físicas, químicas e biológicas. Com relação a esses parâmetros, indique a opção correta.
Provas
Dadas as afirmativas seguintes a respeito dos métodos volumétricos de análises,
I. Indicadores são frequentemente adicionados a solução a ser analisada para produzir uma mudança física observável, que sinaliza o ponto final ou a proximidade do ponto de equivalência em uma titulação.
II. Um padrão primário é uma substância de alta pureza, que é utilizada como referência para uma titulação ou outros tipos de análises quantitativas.
III. O pH onde ocorre o ponto de equivalência na titulação de um ácido com uma base, é sempre próximo a 7,0, independentemente da força do ácido e da base envolvidos na titulação.
IV. A leitura do volume correto de uma solução empregada numa titulação, depende da posição do observador em relação a Bureta.
verifica-se que estão corretas apenas
Provas
O processo de coagulação química é uma das etapas do tratamento de água. A respeito deste processo, indique a opção correta.
Provas
Uma amostra de 7,00 g de um pesticida contendo DDT (C14H9Cl5) foi decomposta com sódio metálico usando álcool como solvente. Os íons cloretos liberados na reação foram precipitados como AgCl. Qual o percentual de DDT na amostra, sabendo-se que foram recuperados 0,34 g de AgCl?
Dados: massas atômicas, em g mol-1, H = 1, C = 12, Na = 23, Cl = 35,5 e Ag = 108.
Provas
A reação entre uma porção de bicarbonato de sódio e uma solução aquosa de ácido clorídrico é representada pelas curvas de produção de dióxido de carbono em função do tempo. Para avaliar esta reação, foram realizados diversos experimentos:
(1) usou-se NaHCO3 na forma de pó fino e um tablete de massa igual a do pó fino;
(2) usou-se NaHCO3 na forma de pó fino em duas temperaturas diferentes;
(3) usou-se NaHCO3 na forma de pó fino, com adição de soluções aquosas de HCl de concentrações diferentes.
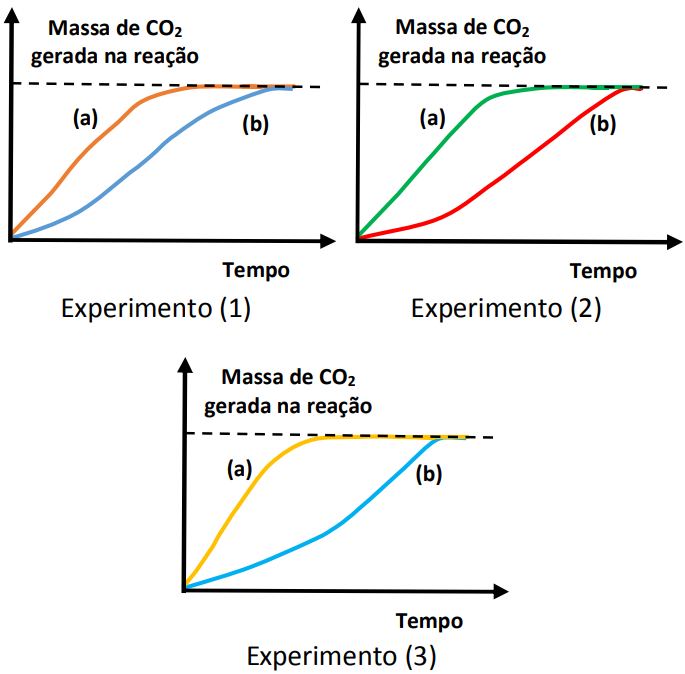
Para análise dos experimentos, considere que as demais condições experimentais foram mantidas idênticas, exceto quando mencionado na descrição do teste. A partir dos experimentos foram elaboradas as seguintes declarações:
I. no experimento 1, a curva (a) corresponde ao teste com NaHCO3 na forma de pó fino;
II. no experimento 2, a curva (a) corresponde ao teste realizado com temperatura menor que no teste (b);
III. no experimento 3, a curva (b) corresponde ao teste realizado com uma concentração de HCl menor do que no teste (a);
IV. a velocidade da reação de decomposição do NaHCO3 com HCl depende apenas das concentrações dos reagentes e da temperatura.
Dos itens acima, verifica-se que estão corretas apenas
Provas
- FundamentosTransformações: Estados Físicos e Fenômenos
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Dadas as afirmativas a respeito das características físico-químicas da água,
I. A dureza da água indica a concentração total de cátions de cálcio e magnésio presentes na amostra.
II. A dureza da água é expressa em miligramas de CaCO3 por litro.
III. A dureza da água melhora a eficiência de sabões e detergentes e evita a formação de incrustações em tubulações.
IV. A alcalinidade da água pode ser definida como uma medida da habilidade de neutralizar ácidos.
verifica-se que estão corretas apenas
Provas
Dada a reação a seguir,
20 HNO3 + 3 P4 + 8 H2O → 12 H3PO4 + 20 NO
verifique qual opção está correta.
Provas
O conceito de Energia Livre foi introduzido pelo físico-químico Josiah Willard Gibbs. Numa reação química, esta energia livre liberada representa a energia
Provas
Qual dos pares abaixo apresenta óxidos com ligações covalente e iônica, respectivamente?
Provas
Considere os seguintes átomos: A, B e C. O átomo A possui número atômico 28 e número de massa igual a 58. O átomo C possui número atômico 26.
Sabendo que A e B são isótopos, A e C são isótonos e B e C são isóbaros, qual o número de nêutrons de B?
Provas
Caderno Container