Foram encontradas 60 questões.
O ozônio tem grande importância nos processos que ocorrem na troposfera. Um mecanismo proposto para a sua decomposição na atmosfera, na ausência de poluentes, é apresentado a seguir:
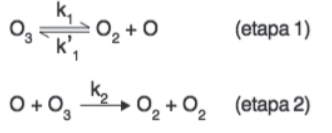
Considerando que a etapa lenta do processo é a 2, qual é a relação de dependência existente entre a velocidade de decomposição do ozônio e as concentrações das espécies envolvidas?
Provas
O diagrama de van Arkel-Ketelar apresenta uma visão integrada das ligações químicas de compostos binários, representando os três tipos clássicos de ligação nos vértices de um triângulo. Os vértices esquerdo e direito da base correspondem, respectivamente, aos elementos menos e mais eletronegativos, enquanto o vértice superior do triângulo representa o composto puramente iônico.
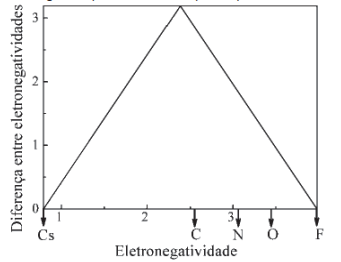
Com base no diagrama, assinale a alternativa que apresente o composto binário de maior caráter covalente.
Provas
O catalisador é uma substância que aumenta a velocidade de uma reação química sem que ela própria seja consumida ou modificada nessa reação. Há vários modos de um catalisador fornecer um caminho favorável para uma reação orgânica. Acerca desses modos, assinale a alternativa correta.
Provas
No tipo de mistura complexa de gases que podemos encontrar no ar urbano, muitas reações químicas podem ocorrer. Por exemplo, o NO2 pode reagir com o ozônio, de acordo com a seguinte equação química:
NO2 (g) + O3 (g) → NO3 (g) + O2 (g)
Considere os seguintes dados para a cinética dessa reação:
Experimento | [NO2] inicial (mol L-1) | [O3] inicial (mol L-1) | Velocidade inicial (mol L-1 s-1) |
1 | 2,3 x 10-5 | 3,0 x 10-5 | 1,0 x 10-5 |
2 | 4,6 x 10-5 | 3,0 x 10-5 | 2,1 x 10-5 |
3 | 4,6 x 10-5 | 6,0 x 10-5 | 4,2 x 10-5 |
O valor da constante de velocidade para essa reação, em L/mol.s, é igual a
Provas
Os átomos de iodo combinam-se para formar iodo molecular em fase gasosa de acordo com:
I(g) + I(g) → I2(g)
A reação precedente segue uma cinética de segunda ordem e possui uma constante de velocidade de 7,0 x 109 M-1.s-1 a 23ºC. Nas alternativas a seguir, assinale o tempo de meia-vida, em segundos, da reação quando a concentração inicial de I for de 0,60 M e de 0,42 M.
Provas
O ferro em uma amostra de minério de ferro pode ser convertido quantitativamente em íon ferro(II), Fe2+, em uma solução aquosa, e essa solução pode ser então titulada com solução de permanganato de potássio, KMnO4. A equação iônica líquida balanceada para a reação que ocorre no decorrer dessa titulação é apresentada a seguir:
MNO4 - (aq) + 5 Fe+2(aq) + 8 H3O+(aq) → Mn+2 + 5 Fe+3(aq) + 12 H2O(l)
Uma amostra de 1,026 g do minério que contém ferro requer 24,35 mL de KMnO4 0,0195 M para alcançar o ponto de equivalência. Qual o teor de ferro, em % massa, presente na amostra de minério?
Provas
Soluções tampão são importantes em diversos estudos, uma vez que o funcionamento apropriado de muitos sistemas depende do pH. Nas alternativas a seguir, aponte o pH de uma solução constituída por KH2PO4, numa concentração de 0,200 mol.L-1 e K2HPO4, sob concentração de 0,100 mol.L-1.
(Dados: pKa do íon H2PO4 − é 7,21; log 2 = 0,3.)
Provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Calcular a solubilidade do cromato de prata, Ag2CrO4, em mol.L−1 presente em uma solução de nitrato de prata, AgNO3, 0,010 mol.L-3.
(Dado: Kps = 2,0x10−12)
Provas
Suponha que uma mistura SO2, O2 e SO3 esteja em equilíbrio a 852 K.
2 SO2 (g) + O2 (g) → 2 SO3(g)
As concentrações de equilíbrio são [SO2] = 3,61 x 10-3 mol/L, [O2] = 6,11 x 10-4 mol/L e [SO3] = 1,01 x 10-2 mol/L. Assim sendo, a constante de equilíbrio calculada desse equilíbrio, na temperatura dada, será
Provas
O MTBE (éter-tert-butilmetílico) tem sido usado como aditivo na gasolina. O composto é produzido pela reação do metanol com o isobuteno, de acordo com a seguinte equação:
CH3OH + (CH3)2C=CH2 → (CH3)3COCH3
Se deixarmos 45,0kg de metanol reagir com 70,0kg de isobuteno, assinale a alternativa que apresente a massa em grama de MTBE obtida.
Provas
Caderno Container