Foram encontradas 40 questões.
Em um frasco, colocam-se 1,0 mol de SO2 e 1,0 mol de O2, a 400 K. Quando o equilíbrio é alcançado, o frasco reacional contém 0,6 mol de SO3 e as correspondentes quantidades remanescentes de SO2 e O2, de acordo com a reação abaixo:
!$ \mathsf{2~SO_2(g)~+~O_2(g)~\leftrightarrows~2~SO_3(g)} !$
O número total de mols dos gases no equilíbrio é:
Provas
Questão presente nas seguintes provas
A aspirina é um medicamento largamente usado como analgésico e seu nome químico é ácido acetilsalicílico. Acredita-se que suas propriedades analgésicas se devem ao ácido salicílico, C6H4(OH)CO2H, formado pela decomposição do ácido acetilsalicílico no estômago.
Considere a solubilidade do ácido salicílico sendo 1,09 g em 500 mL de água.
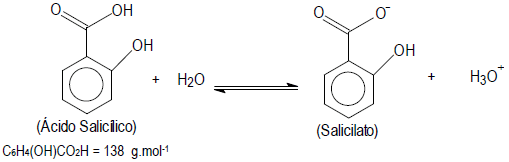
A concentração molar dessa solução e o efeito da diminuição do pH sobre o equilíbrio, mostrado acima, são, respectivamente:
Provas
Questão presente nas seguintes provas
A tabela periódica atual está organizada tendo por base a ordem crescente do número atômico dos elementos, classificando-os em famílias e períodos, em função da distribuição eletrônica e do número quântico principal da camada de valência.
Sobre o assunto, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Se o conjunto de números quânticos n = 3, !$ \ell=1 !$ e m = 0 descreve o comportamento do elétron de valência de um átomo X, no estado fundamental, então X é um calcogênio.
( ) Um elemento Y que nas condições ambientes se encontra no estado líquido é formado por átomos representados por 35Y80. Y apresenta 7 elétrons na camada de valência.
( ) A configuração eletrônica de um átomo neutro no estado fundamental é 1s2 2s2 2p6 3s2 3p2; o número de orbitais vazios remanescentes no nível principal M desse átomo é 6.
( ) Um cátion diatômico A2+ apresenta a configuração eletrônica 3s2 3p6 para o último nível; o número atômico do elemento A é igual a 18.
Assinale a sequência correta.
Provas
Questão presente nas seguintes provas
A Lei n.º 11.892, de 29 de dezembro de 2008, institui a Rede Federal de Educação Profissional, Científica e Tecnológica, cria os Institutos Federais de Educação, Ciência e Tecnologia, e dá outras providências. Em relação aos objetivos dos Institutos Federais, conforme determina essa lei, considere:
I- Ministrar educação profissional técnica de nível médio; prioritariamente na forma de cursos integrados, para os concluintes do ensino fundamental e para o público da educação de jovens e adultos.
II- Ministrar cursos de formação inicial e continuada de trabalhadores, objetivando a capacitação, o aperfeiçoamento, a especialização e atualização de profissionais, em todos os níveis de escolaridade, nas áreas de educação profissional e tecnológica.
III- Realizar pesquisas aplicadas, estimulando o desenvolvimento de soluções técnicas e tecnológicas, estendendo seus benefícios à comunidade.
IV- Desenvolver atividades de extensão com a finalidade de fornecer à comunidade em geral espaço com infraestrutura para o seu entretenimento.
São objetivos dos Institutos Federais:
Provas
Questão presente nas seguintes provas
A reação química entre o óxido de cálcio e o cloreto de amônio leva à formação de NH3, de acordo com:
!$ \mathsf{CaO(s)~+~2~NH_4CI(s)~\rightarrow~2~NH_3(g)~+~H_2O(g)~+~CaCl_2(s)} !$
Considere a reação entre 112 g de CaO e 220 g de NH4Cl e calcule:
I- A massa de amônia obtida na reação, se o rendimento for 100%.
II- O rendimento percentual dessa reação, se a massa de NH3 obtida for 60 g.
Dados: CaO = 56 g.mol-1; NH4Cl = 53,5 g.mol-1; NH3 = 17 g.mol-1; H2O = 18 g.mol-1 e CaCl2 = 111 g.mol-1
Marque a alternativa que apresenta corretamente os resultados obtidos em I e II, respectivamente.
Provas
Questão presente nas seguintes provas
A Constituição Federal da República, em seu Capítulo III, seção I, Art. 208, estabelece que o dever do Estado com a educação será efetivado mediante a garantia de
Provas
Questão presente nas seguintes provas
A obtenção do gás de síntese (CO + H2) pode ser representada pela equação química abaixo, cuja energia de Gibbs padrão de reação !$ (\Delta_ r G^o) !$ é + 91,4 kJ.mol-1.
!$ \mathsf{C(s,grafite)~+~H_2O(g)~\rightarrow~CO(g)~+~H_2(g)} !$
Analise essa reação com base nos dados constantes da tabela a seguir.
| Dados (298 K) | !$ S^o_m~\mathsf{(J.K^{-1}.mol^{-1})} !$ | !$ \Delta_ f H^o~\mathsf{(kJ.mol^{-1})} !$ |
|
C(s,grafite) H2O(g) CO(g) H2(g) |
5,7
188,8
197,7
130,7
|
0
-241,8
-110,5
0
|
A partir das informações dadas e da análise, assinale a afirmativa correta.
Provas
Questão presente nas seguintes provas
Trabalhando em sala de aula com atividades relativas ao estudo de textos, o professor identifica em alguns alunos grande dificuldade no desenvolvimento do trabalho. Orienta aos alunos que trabalhem em pequenos grupos para discutirem, debaterem e socializarem a compreensão do texto. Identifica que, dessa forma, os alunos conseguem assimilar melhor o significado do texto e apresentam ótimo desempenho em relação à atividade dada. Com essa prática, o professor revela conceber o conhecimento na perspectiva
Provas
Questão presente nas seguintes provas
A história das ideias educacionais no Brasil é marcada por um conjunto de tendências que dão suporte à organização e gestão do trabalho pedagógico na escola. A par disso, o momento atual vem sendo caracterizado pela necessidade de rompimento com o burocratismo, autoritarismo, rotinas rígidas em favor de uma prática pedagógica que favoreça a participação, o trabalho coletivo, a criatividade, a inovação e a valorização da diversidade. Um professor comprometido com esses princípios desenvolverá o seu trabalho ancorado
Provas
Questão presente nas seguintes provas
A hidratação é um dos principais tipos de reações químicas. Todos os óxidos de metais alcalinos terrosos, exceto o BeO, reagem com água formando hidróxidos iônicos. A velocidade dessa reação aumenta com a dimensão do íon metálico e depende também do pré-tratamento que o óxido tenha sofrido. A hidratação do óxido de um metal alcalino terroso do 3º período produz um composto X.
Sobre essa reação de hidratação, pode-se afirmar:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container