Foram encontradas 40 questões.
Uma amostra de 5 g de Alumínio (Al) e uma amostra de 5 g de ferro (Fe) foram aquecidas de 30°C para 100°C. Qual dos metais absorveu a maior quantidade de calor? Assinale a alternativa CORRETA:
Provas
Qual das seguintes espécies não tem entalpia padrão de formação igual a zero (∆Hf 0 = 0), a 250C? Assinale a resposta CORRETA:
Provas
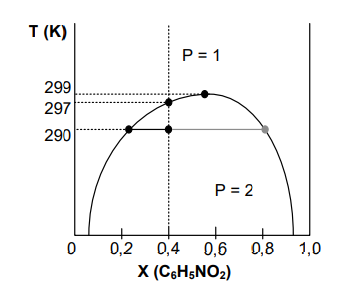
A figura abaixo representa o diagrama de fases (líquidos parcialmente miscíveis) de uma mistura de 50 g de hexano (0,6 mol de C6H14) e 50 g de nitrobenzeno (0,4 mol de C6H5NO2), preparada a 290 K e 1 atm. Com base no diagrama de fases, assinale a alternativa CORRETA que indica a temperatura da mistura para que a amostra tenha uma só fase:
Provas
Assinale a alternativa CORRETA que indica quantos gramas de cloreto de sódio (NaCl) devem ser adicionados a 600 g de água para resultar em uma solução com uma pressão de vapor 3,2 mmHg abaixo da pressão de vapor da água a 30°C. (A pressão de vapor da água a 30°C é 31,8 mmHg.)
Provas
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Dois líquidos A e B têm pressões de vapor de 80 mmHg e de 150 mmHg, respectivamente, a 25°C. Para uma mistura de 2 mols de A e 6 mols de B, assinale a resposta CORRETA que indica a pressão de vapor da solução ideal preparada:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Química InorgânicaReações Inorgânicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Inúmeras grutas calcárias em muitas regiões do Brasil exibem formações esculturais chamadas de estalactites. São essas formações que dão extraordinária beleza às grutas calcárias, transformando-as em atrações turísticas. Estas formações podem ser representadas pela seguinte reação reversível:
CaCO3(s) + CO2(g) + H2O(l) ↔ Ca2+ (aq) + 2HCO3 - (aq)
Com relação à formação das estalactites, avalie cada uma das afirmativas abaixo:
I. O interior das cavernas com essas formações contém ar com um alto teor de gás carbônico liberado a partir da decomposição de bicarbonato de cálcio, que volta à forma de carbonato de cálcio cristalino (calcita).
II. A formação das estalactites ocorre através da infiltração das águas superficiais ou de lençóis de água subterrânea, carregadas de bicarbonato de sódio, que afloram no teto, de onde gotejam.
III. O pH da água das chuvas da região não influencia no fenômeno de formação das estalactites.
IV. O aumento da temperatura no interior da caverna favorece a decomposição das estalactites, diminuindo a concentração de gás carbônico no local.
Está(ão) CORRETA(S) a(s) seguintes afirmativas:
Provas
Para reagir completamente com uma massa de 45,00 g de um ácido desconhecido, HxA, foram gastos 280,00 mL de uma solução aquosa de NaOH 2,51 mol/L, que reagem de acordo com a seguinte equação não balanceada:
HxA(aq) + xNaOH(aq) ↔ Na3A(aq) + 3H2O(l)
A massa molar do ácido em g/mol será:
Provas
A opção que traz o método mais adequado para o preparo de 1,00 L de HCl(aq) em uma concentração de 0,175 mol/L é:
Provas
“O ácido cítrico é o responsável pela acidez de frutas cítricas. Para emprego industrial, o ácido cítrico é fabricado pela fermentação aeróbica do açúcar bruto (sacarose) ou açúcar de milho (dextrose) por uma casta especial de Aspergillus niger. Seu maior emprego é como acidulante em bebidas carbonatadas e alimentos. No campo médico, é empregado na fabricação de citratos e de sais efervescentes”.
Disponível em: <http://qnesc.sbq.org.br/online/qnesc15/v15a02.pdf>. Acesso em: 05 out. 2016.
Determine o número de mol de ácido cítrico (C6H8O7) presente em um litro de refrigerante, que após análise de uma amostra de 100 mL, apresentou uma massa de 0,12 g de ácido cítrico.
Provas
A hematita (Fe2O3) é o principal minério de ferro encontrado na natureza, e um dos seus empregos é na obtenção do ferro elementar, a partir da seguinte reação (não balanceada):
Fe2O3 + CO → Fe + CO2
Determine a massa de Fe2O3 necessária para produzir 1,50 toneladas (t) de Fe.
Provas
Caderno Container