Foram encontradas 40 questões.
Os líquidos A e B são misturados. O vapor acima dessa mistura contém ambos os compostos. A mistura obedece à lei de Raoult. O valor da pressão total (p) é 72 kPa quando a fração molar de A (xA) é 0,3 e 80 kPa quando a mistura é equimolar.
As pressões de vapor de A e B, respectivamente, em kPa, serão de
Provas
Questão presente nas seguintes provas
Numa empresa de produção de óleo, desejamos efetuar a separação de todos os componentes de uma mistura hipotética (Tabela 4) utilizando uma centrífuga decantadora vaso tubular (Figura 7).
Tabela 4: Componentes de uma mistura hipotética
| Componente |
Densidade absoluta
(Kg/ m3)
|
Composição
(%p/p)
|
|
| 1 | Água | 1,000 | 90,0 |
| 2 | Óleo | 0,787 | 9,5 |
| 3 |
Gomas, pelos,
sólidos, etc.
|
Aproximadamente 1,150 | 0,5 |
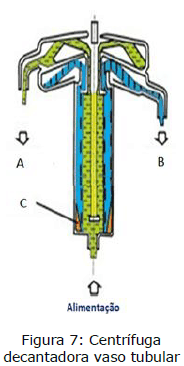
Considerando os dados apresentados, os pontos de coleta dos diferentes componentes serão
Provas
Questão presente nas seguintes provas
As emissões de gases causadoras do efeito estufa ameaçam o equilíbrio do planeta ao promoverem o aquecimento global. A emissão de dióxido de carbono (CO2) pelos veículos é um dos principais responsáveis. Um carro de passeio típico roda 80 km por dia e seu consumo é de 10 km por litro de gasolina, a qual é uma mistura de hidrocarbonetos. Para esse problema, vamos supor que a gasolina seja composta somente de isooctano, C8H18. Quando o isooctano queima totalmente, combina-se com o oxigênio, para produzir dióxido de carbono e água, segundo a seguinte reação química:
C8 H18 + X O2 → Y CO2 + Z H2O
Um dos parâmetros de desempenho mais importante de um motor de combustão interna é a razão entre combustível e ar nesta mistura. Em uma situação ideal, a mistura deve conter a quantidade de oxigênio estritamente necessária para queimar todo o combustível presente. A razão entre massa de ar e massa de combustível nessas condições é chamada de razão estequiométrica (RE). Sabendo que o ar contém 23,2% em massa de oxigênio (32 g.mol-1), considerando que a massa molecular da gasolina é de 114 g.mol-1 e que sua massa específica é de 0,75 kg.L-1, julgue as seguintes afirmações com relação ao texto.
I. O valor de RE é cerca de 15.
II. O valor de RE é menor do que X, mas é maior do que o valor de Y.
III. A massa de gasolina queimada por ano é menor do que 2000 kg.
IV. O valor de Y é 8 e é menor do que o valor de Z.
Está (ão) correta(s) apenas as afirmativas
Provas
Questão presente nas seguintes provas
O número de pratos teóricos de uma coluna de destilação para uma mistura de benzeno-tolueno foi calculado utilizando a resolução gráfica de McCabe-Thiele, considerando-se as hipóteses a seguir:
- a coluna não apresenta fugas térmicas;
- a coluna opera a pressão de 760 mmHg, sendo todas as quedas de pressão, dentro da coluna, desprezíveis;
- a composição molar da alimentação é de 47% de benzeno, estando hipoteticamente numa temperatura e pressão que fazem a mistura encontrar-se no estado de líquido saturado;
- o condensador total condensa todo o vapor sem resfriar o condensado abaixo de seu ponto de ebulição;
- o calor fornecido à mistura é efetuado por um refervedor parcial e considerado como um prato de separação.
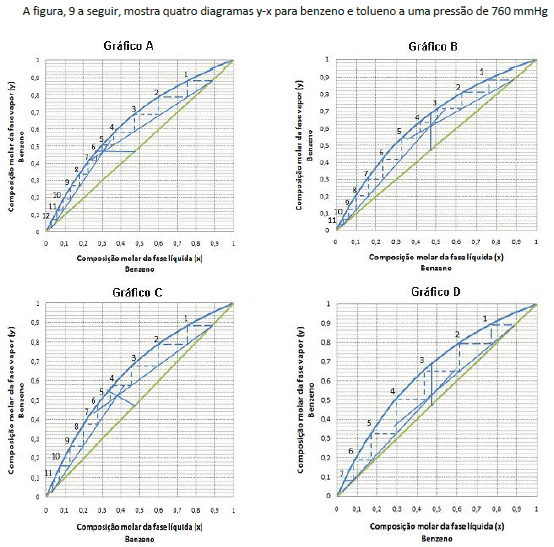
Figura 9: Diagramas y-x para benzeno e tolueno a uma pressão de 760 mmHg, usados na determinação do número teórico de pratos, através do método de resolução gráfica de McCabe-Thiele.
Sabendo que a coluna real possui 14 pratos e considerando as observações anteriormente mencionadas, a eficiência global aproximada da coluna e o gráfico que melhor representa a resolução por McCabe-Thiele são
Provas
Questão presente nas seguintes provas
Especificamente quanto à transferência de calor por convecção, o que é correto afirmar?
Provas
Questão presente nas seguintes provas
As equações de estado são utilizadas para descrever o comportamento de gases quando submetidos a transformações termodinâmicas. Uma equação bastante usada é a equação de Van Der Waals:
!$ p = { \large RT \over V-b} - { \large a \over V^2} !$
onde a,b e R são constantes, p é a pressão, T é a temperatura absoluta, e V é o volume molar do gás.
Comparando a equação de van der Waals com a equação dos gases ideais, afirma-se:
I. A equação dos gases perfeitos descreve o comportamento desses fluidos em escala macroscópica, desconsiderando interações intermoleculares.
II. A equação de van der Waals procura quantificar os efeitos de não-idealidade dos gases com o uso de três constantes diferentes para cada gás.
III. A constante “a”, na equação van der Waals, representa a força de atração entre as moléculas, corrigindo, grosso modo, o volume total do sistema.
IV. A constante “b”, da equação de van der Waals, leva em conta o volume ocupado por cada molécula, corrigindo neste caso o volume total de gás.
Estão corretas apenas as afirmativas
Provas
Questão presente nas seguintes provas
Para expressão diferencial da energia interna:
dU = Tds - PdV
onde T, S P, e V são, respectivamente, temperatura, entropia, pressão e volume.
A relação de Maxweel desenvolvida a partir dessa expressão é:
Provas
Questão presente nas seguintes provas
No processo de fabricação de açúcar, imediatamente antes da etapa de filtração, adiciona-se bagacilho à calda, numa relação de 5 Kg por tonelada de calda. A finalidade do bagacilho é atuar como auxiliar de filtração.
Afirma-se que sua presença
Provas
Questão presente nas seguintes provas
A questão refere-se à figura 11, a seguir:
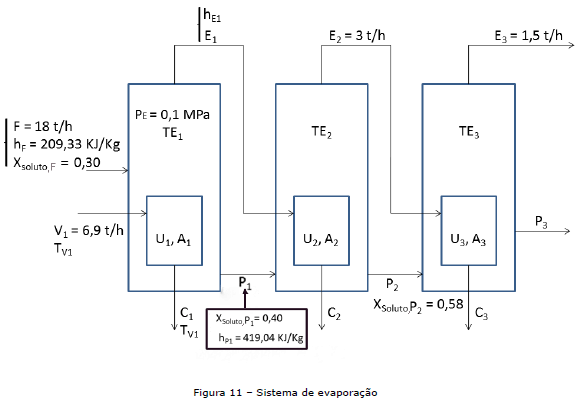
Legenda:
F, E1, E2, E3, P1, P2, P3, V, C1, C2, C3 = vazões mássicas em toneladas por hora;
XSoluto = frações mássicas de soluto nas diferentes correntes;
hF, hE1, hP1 = entalpias dos fluidos nas correntes F, E1 e P1, respectivamente , em KJ/Kg;
TE1, TE2, TE3 = temperaturas no interior dos evaporadores 1, 2 e 3, respectivamente, em °C;
TV1 = temperatura do vapor de aquecimento e do condensado produzido no primeiro efeito, em °C;
PE = pressão no interior do evaporador 1 em MPa;
U1, U2, U3 = Coeficientes globais de troca térmica dos evaporadores 1, 2 e 3, respectivamente, em Kcal/h.m2.°C;
A1, A2, A3 = áreas de troca térmica dos evaporadores 1, 2 e 3, respectivamente, em m2.
Considerando os dados apresentados na figura 11, a economia ou eficiência desse sistema será de aproximadamente
Provas
Questão presente nas seguintes provas
A lei de Stokes é corretamente representada pela equação:
!$ V_S = { \large D^2_p × g × (ρ_s - ρ_f) \over 18 × μ} !$
Observação: “VS” corresponde à velocidade de sedimentação, “Dp”, ao diâmetro das partículas; “g” à aceleração da gravidade; !$ ρ_s !$ à massa especifica das partículas sólidas; !$ ρ_f !$ à massa específica do fluido; e !$ μ !$ à viscosidade dinâmica do fluido. Considerando essa equação, é correto afirmar que
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container