Foram encontradas 60 questões.
Determine o volume de amônia, nas CNTP, produzido a partir de 140 g de gás nitrogênio e o número de mol de amônia produzido a partir 5 mol de gás nitrogênio, ambos com quantidade suficiente de gás hidrogênio.
N2(g) + H2(g) → NH3(g)
Provas
Considere a decomposição térmica de 245 g de KCℓO3 e determine a massa de O2 produzida juntamente com 149 g de KCℓ.
Provas
Analise a figura representativa de uma célula eletroquímica e assinale a alternativa correta.
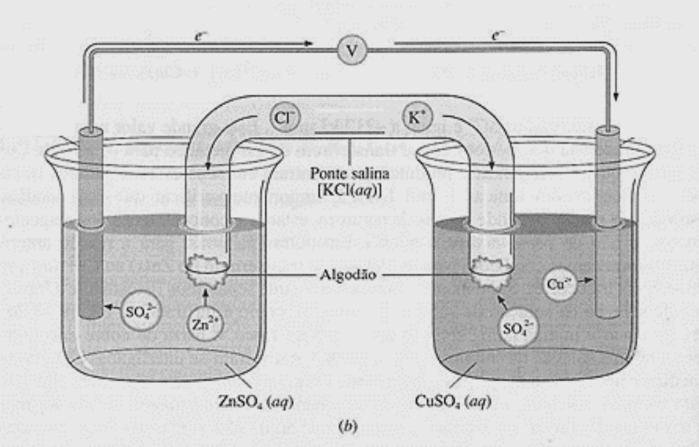
Fonte: Adaptado de Russel (1994).
Provas
A eletroquímica é a parte da química que estuda a produção de corrente elétrica por meio de reações químicas (pilhas e baterias) e o processo inverso a esse (eletrólise). Sobre isso, analise as assertivas abaixo, assinalando V, se verdadeiras, ou F, se falsas.
( ) O ânodo é o eletrodo no qual ocorre a oxidação numa célula eletroquímica.
( ) Numa célula eletroquímica, os elétrons fluem do cátodo para o ânodo.
( ) O cátodo é o eletrodo no qual ocorre a redução numa célula eletroquímica.
( ) Numa célula eletroquímica, o cátodo, por apresentar carga negativa, recebe os elétrons do ânodo, ou seja, os elétrons migram do polo positivo para o polo negativo.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Uma maneira muito comum, mas menos precisa, de determinar o pH de uma solução é por meio do uso de indicadores, que são substâncias que mudam de cor em função da concentração de H+ e OH-, ou seja, de acordo com o pH. Existem vários indicadores ácido-base, inclusive naturais, como o suco do repolho roxo que, em uma solução neutra, apresenta coloração roxa. Porém, quando ocorre mudança de pH, sua coloração pode variar do vermelho (meio ácido) ao verde-amarelado (meio básico). Analise o comportamento das soluções na presença do indicador natural e assinale a alternativa INCORRETA:
Provas
Um indicador é um par conjugado de ácido e base de Brönsted-Lowry cujo ácido apresenta uma coloração, e a base, outra. Pelo menos uma das colorações é suficientemente intensa para ser visualizada em soluções diluídas. A maioria dos indicadores são moléculas orgânicas com estruturas relativamente complexas, e um indicador comum é a fenolftaleína. Sobre isso, analise as assertivas abaixo:
I. A concentração de um indicador em solução é geralmente tão baixa que sua influência sobre o pH da mesma é desprezível.
II. A forma ácida HIn da fenolftaleína é incolor.
III. Uma solução com pH 4,0 apresentará coloração vermelha com a adição de fenolftaleína.
Quais estão corretas?
Provas
Determine o pH de uma solução-tampão preparada a partir de uma solução de ácido acético, 0,1 mol∙L-1, contendo uma solução de acetato de sódio, 0,5 mol∙L-1 e assinale a alternativa correta. Dados: Ka do ácido acético = 1,8∙10-5; log 1,8 = 0,25 e log 5 = 0,7.
Provas
Em laboratórios, a maneira mais precisa de determinar o pH de uma solução é por meio da utilização de um aparelho elétrico denominado pHmetro. Com o uso do pHmetro, pode-se determinar o pH de alguns materiais comuns em nosso dia a dia, conforme tabela apresentada abaixo:
Solução | pH |
Suco de limão | 2,0 |
Vinagre | 2,8 |
Suco de laranja | 3,5 |
Café | 5,0 |
Leite | 6,4 |
Sangue | 7,4 |
Água do mar | 8,5 |
Leite de magnésia | 10,5 |
Alvejante | 12,0 |
Assinale a alternativa correta de acordo com a tabela acima.
Provas
Os valores das constantes de ionização de muitos ácidos já foram determinados experimentalmente e encontram-se tabelados à mesma concentração e temperatura. Por meio dos valores tabelados, pode-se comparar a força desses ácidos. Analise a tabela a seguir e assinale a alternativa INCORRETA.
Acidez de alguns ácidos
ÁCIDOS | Constante de ionização (Ka) |
HCl | 10+7 |
H2SO4 | 10+3 |
H2SO3 | 1,5.10-2 |
H3PO4 | 7,6.10-3 |
HNO2 | 4,3.10-4 |
HF | 3,5.10-4 |
CH3COOH | 1,8.10-5 |
H2CO3 | 4,3.10-7 |
H2S | 1,3.10-7 |
HCN | 4,9.10-10 |
Fonte: Adaptado de ATKINS e JONES (2011).
Provas
Em relação a constante de equilíbrio, é correto afirmar:
Provas
Caderno Container