Foram encontradas 50 questões.
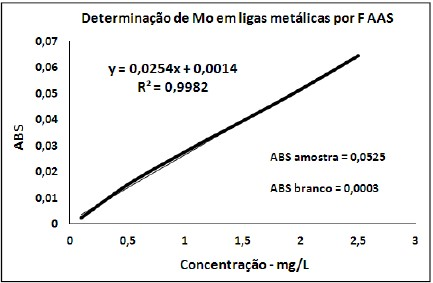
Para determinar o molibdênio por FAAS em uma liga metálica deve-se realizar o seguinte procedimento: dissolver 10,0 mg de amostra moída e peneirada com 5,0 mL de água régia em chapa aquecedora. Após resfriamento, é necessário transferir quantitativamente a solução para um balão de 25 mL e ajustar o volume com água deionizada. Em seguida, transferir uma alíquota de 5,0 mL para um balão volumétrico de 10 mL e ajustar o volume com água deionizada. As medidas foram realizadas em um espectrômetro após a construção da curva analítica, utilizando chama de acetileno/óxido nitroso. As absorvâncias (ABS) medidas foram: ABSamostra = 0,0525 e ABSbranco = 0,0003. Considerando-se as absorvâncias medidas e a curva de calibração a seguir, qual é o teor de molibdênio na liga metálica?
Provas
A titulação ácido-base ou volumetria de neutralização é comumente empregada para diversas finalidades em laboratórios de ensino, pesquisa e prestadores de serviços. Sobre a volumetria de neutralização e suas aplicações é INCORRETO afirmar que
(Considere os dados das constantes de dissociação do H3PO4: Ka1 = 7,5 x 10–3; Ka2 = 6,2x 10–8; Ka1 = 5,0 x 10–13.)
Provas
Observe um típico instrumento de absorção atômica de duplo feixe. A técnica de espectrometria de absorção atômica com chama (FAAS) é bastante utilizada em laboratórios de análises clínicas, de alimentos, controle de qualidade de estações de tratamento de água e outros.
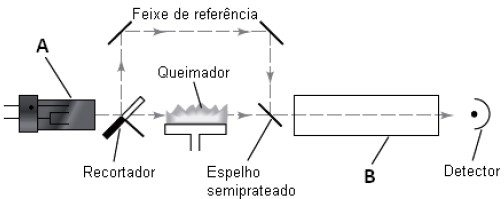
(Skoog D. A., West D. M., Holler F. J. e Crouch S. R. Fundamentos de Química Analítica. 8ª Ed. São Paulo: Pioneira Thomson Learning, 2006. – Com adaptações.)
Assinale a sequência da figura anterior que apresenta uma aplicação da FAAS para análises de parâmetros de qualidade da água.
Provas
Certo laboratório recebeu um lote de minério para que se determinasse o teor de Fe. O técnico responsável pela análise partiu de 6,7200 g de amostra e, após o devido tratamento, obteve 480 mg de precipitado incinerado. Qual é a porcentagem (massa/massa) de ferro na amostra? (Considere massas molares (g mol–1): Fe = 56; O = 16.)
Provas
Um laboratório recebeu um lote de amostra, retirada próxima a uma mineradora, para a realização de uma série de análises, dentre elas a determinação de Fe3+. O técnico responsável transferiu uma alíquota de 5,00 mL para um balão de 50,0 mL e adicionou SCN– em excesso para a formação do complexo colorido FeSCN2+. Após ajustar o volume com água deionizada, ele mediu a absorbância da solução em uma cubeta de 1,00 cm e comprimento de onda de 580 nm. O valor de absorbância obtido foi 0,700. Sabendo-se que a absortividade molar do complexo (\( ε \)) é 7,00 x 103 L mol–1 cm–1, assinale a alternativa correta sobre essa análise e o teor do analito em ppm. (Considere: densidade da solução = 1,00 g mL–1; A = \( ε \)bc; massa molar do Fe = 56,0 g/mol–1.)
Provas
Deve-se realizar a titulação de 100 mL das seguintes soluções: solução 0,1 mol/L de uma espécie A (Ka = 10–4) e solução 0,1 mol/L de uma espécie B (Kb = 10–4). Há disponível no laboratório soluções padronizadas de HCl 0,1 mol/L e NaOH 0,1 mol/L, além dos indicadores apresentados na tabela.
|
Indicadores |
Vermelho de cresol | Vermelho de metila | Fenolftaleína |
Amarelo de alizarina |
|
pH de transição |
0,2 – 1,8 | 4,2 – 6,3 | 8,3 – 10 |
10 – 12 |
Considere:
\( \bullet pH=\dfrac{1}{2}pK_w+\dfrac{1}{2}pK_a-\dfrac{1}{2}pC\,\,e\,\,pH=\dfrac{1}{2}pK_w-\dfrac{1}{2}pK_b+\dfrac{1}{2}pC, \) onde C = concentração da espécie conjugada.
\( \bullet pX = log[X]; - log [0,05] = 1,3; -log [10^{–X}] = X; K_w = 10^{–14} \)
Assinale a alternativa que apresenta corretamente o procedimento a ser adotado.
Provas
Um estudante preparou uma solução da seguinte maneira: dissolução de 0,48004 g de soluto em 25 mL de ácido 50% v/v e ajuste do volume com água para 100 mL. Qual é a concentração da solução preparada?
(Considere massa molar do soluto = 480,04 g mol–1.)
Provas
Um químico, responsável por um laboratório que presta serviços na área de análises ambientais, avaliou o desempenho de quatro técnicos. Para isso, pediu que cada técnico fizesse, separadamente, a determinação de Cd em uma amostra de minério e lhe fornecesse o resultado. Os resultados obtidos pelos técnicos encontram-se na tabela a seguir. Observe.
|
Técnico 1 |
2,49 ± 0,02 |
|
Técnico 2 |
2,51 ± 0,50 |
|
Técnico 3 |
2,80 ± 0,01 |
|
Técnico 4 |
2,80 ± 0,50 |
Considere: (média ± desvio; n = 7) – resultados expressos em termos de concentração (mg/Kg)
Ao avaliar os resultados obtidos pelos técnicos, sabendo-se que a amostra possuía uma concentração conhecida de 2,50 mg/kg, o químico concluiu que os resultados obtidos pelo(s)
Provas
Um indivíduo transferiu para um balão de 500 mL as seguintes soluções: 50 mL de NaCl 58,5% m v–1 e 250 mL de CaCl2 0,50 mol L–1. Após ajustar o volume com água deionizada, a solução foi rotulada e devidamente armazenada. Assinale a alternativa que expressa corretamente as concentrações do rótulo.
(Considere massas molares (g/mol): Ca = 40; Cl = 35,5; Na = 23; m v–1 = p v–1)
Provas
O cloreto de iodo (ICl), também denominado monocloreto de iodo, é utilizado como catalisador na titulação de sulfato de cério com oxalato de sódio. Este composto pode ser obtido de acordo com a reação não balanceada: KIO3 + KI + HCl → KCl + ICl + H2O. É necessário preparar 500 mL de solução 0,003 mol L–1 de ICl, a partir dos reagentes mencionados na reação. Assinale a massa de KIO3 que deverá ser utilizada com quantidade estequiométrica de KI e HCl.
(Considere massas molares (g/mol): KIO3 = 214; KI = 166; HCl = 36,5; KCl = 74,5; ICl = 162,5; H2O = 18.)
Provas
Caderno Container