Foram encontradas 100 questões.
50 g de sulfato de sódio foram dissolvidos em água suficiente para formar meio litro de solução. Qual a molaridade desta solução? Dados: SMA= 32, OMA= 16, NaMA= 23
Provas
A um técnico químico foi solicitado o preparo de uma solução de hidróxido de sódio 20% em massa, a partir de 20 g de uma solução 5% em massa desse composto. Qual é a massa de hidróxido de sódio a ser adicionada à soluçãobase?
Provas
Cada grupo funcional confere uma propriedade característica a uma molécula. Sobre as classes e os compostos orgânicos, considere as afirmações a seguir.
I – Os pontos de ebulição dos álcoois são consideravelmente mais baixos do que os dos alcanos correspondentes.
II – Os pontos de ebulição dos éteres são muito mais baixos do que aqueles dos alcoóis de massa molecular comparável, em virtude da ausência de ligações de hidrogênio no líquido.
III – O grupo carbonila na estrutura da cetona confere volatilidade e solubilidade em água muito superior às dos aldeídos de massa molecular comparável.
IV – Os ácidos carboxílicos, no estado líquido, são altamente associados devido a ligações de hidrogênio.
Estão corretas APENAS as afirmações
Provas
O etanol é um álcool que apresenta elevada solubilidade em água. O que justifica essa afirmação?
Provas
I - CH3CH2COCH2CH3
II - HOOC-COOH
III - CH3COOCH2CH3
IV - CH3CH2CH2OCH3
Qual a nomenclatura IUPAC dos compostos acima apresentados pelas fórmulas estruturais condensadas?
| I | II | III | IV |
Provas
Além de sua fração de hidrocarbonetos, o petróleo apresenta uma fração de outros compostos na qual se destacam alguns compostos oxigenados como os ácidos carboxílicos. Qual das seguintes características NÃO é de ácidos carboxílicos?
Provas
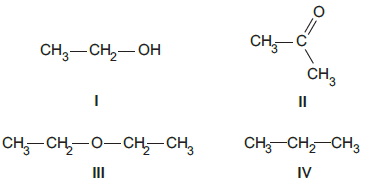
Qual a associação correta entre cada um dos compostos apresentados acima e a função química a que pertencem?
| I | II | III | IV |
Provas
Considere as reações abaixo.
I - N2(g) + 3H2(g) !$ leftrightarrows !$ 2NH3(g)
II - 2C(s) + O2(g) !$ leftrightarrows !$ 2CO(g)
III - CH3OCH3(g) !$ leftrightarrows !$ H2(g) + CH4(g) + CO(g)
Analisando as reações acima quanto ao equilíbrio químico, qual das seguintes conclusões está INCORRETA?
Provas
Zn2+ + 2e− !$ leftrightarrow !$ Zn E0 = -0,76 V
Ag+ + e− !$ leftrightarrow !$ Ag E0 = + 0,80 V
H+ + e− !$ leftrightarrow !$ ½ H2 E0 = 0,00 V
Cu2++ 2e− !$ leftrightarrow !$ Cu E0 = + 0,35 V
Considerando os potenciais-padrão de redução de eletrodos acima, qual é a pilha que fornece maior força eletromotriz?
Provas
Sobre a reação genérica aA+ bB !$ ightleftarrows !$ cC + dD, considere as afirmações a seguir.
I – O aumento da concentração de A, considerando excesso de B no meio, provoca o deslocamento do equilíbrio no sentido de maior geração de D.
II – Sendo A, B, C e D compostos em estado gasoso, e sendo a = b = c = 1 e d = 2, um aumento de pressão favorece o deslocamento do equilíbrio no sentido da direita para a esquerda.
III – A velocidade da reação independe do estado de pulverização dos reagentes.
IV – Supondo que a reação possui etapas intermediárias, deve-se admitir que a velocidade da reação global é igual à da etapa lenta. V – Supondo que a reação se processa sem etapas intermediárias, os expoentes m e n da equação da velocidade v = k[A]m . [B]n são iguais, respectivamente, aos coeficientes da equação a e b.
São corretas APENAS as afirmações
Provas
Caderno Container