Foram encontradas 120 questões.
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Com relação a ligações químicas, geometria molecular e teoria da
ligação de valência, julgue o item que se segue.
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, geometria molecular e teoria da
ligação de valência, julgue o item que se segue.
Uma das principais vantagens da teoria de ligação de valência é a possibilidade de explicar, satisfatoriamente, fenômenos associados a estados de excitação e de prever os espectros de absorção e emissão de energia eletrônica das moléculas.
Uma das principais vantagens da teoria de ligação de valência é a possibilidade de explicar, satisfatoriamente, fenômenos associados a estados de excitação e de prever os espectros de absorção e emissão de energia eletrônica das moléculas.
Provas
Questão presente nas seguintes provas
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

As moléculas se organizam por meio de ligações covalentes entre si para formar os sólidos moleculares.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosTransformações: Estados Físicos e Fenômenos
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Nos líquidos, a ordem de ligação tem mais curto alcance que nos sólidos cristalinos.
Provas
Questão presente nas seguintes provas
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Os sólidos iônicos são cristalinos, e os sólidos moleculares são amorfos.
Provas
Questão presente nas seguintes provas
O ano de 2019 foi proclamado o Ano Internacional da Tabela
Periódica pela Organização das Nações Unidas (ONU). Com
relação à Tabela Periódica, seus elementos químicos e os
modelos atômicos, julgue o item que se segue.
Mendeleev foi o primeiro cientista a organizar os elementos químicos em uma ordem periódica.
Mendeleev foi o primeiro cientista a organizar os elementos químicos em uma ordem periódica.
Provas
Questão presente nas seguintes provas
O policloreto de vinila (PVC) é um polímero com ampla
gama de aplicações, desde a construção civil até a medicina. O
monômero do PVC é o cloreto de vinila (cloroeteno) — C2H3Cl.
A cloração direta do eteno seguida da pirólise é um dos principais
mecanismos para a obtenção do monômero, de acordo com as
seguintes etapas.
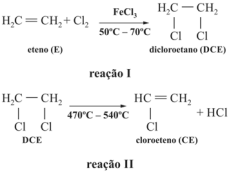
O FeCl3 altera a constante da equação de velocidade da reação I.
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
Margarinas que contêm gorduras vegetais parcialmente
hidrogenadas são frequentemente rotuladas como “feitas com
óleo 100% vegetal”, o que sugere aos consumidores que elas são
muito mais saudáveis que manteiga. No entanto, algumas
ligações duplas dos ácidos graxos no óleo são convertidas da
configuração cis para a configuração trans. Foi demonstrado que
o consumo de alimentos contendo ácidos graxos trans, como as
margarinas, aumenta os níveis de colesterol no sangue.
A equação química a seguir ilustra a adição de H2 a uma
dupla ligação de um ácido graxo.
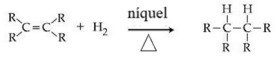
Sabendo-se que o ácido graxo poli-insaturado ômega-6, essencial na dieta humana, é o ácido linoleico, cuja nomenclatura oficial é ácido 9-12-octadecadienoico, é correto afirmar que esse ácido possui nove carbonos e duas insaturações em sua estrutura molecular e que sua fórmula química é a seguinte. CH3–(CH2)4–CH=CH–CH2–CH=CH–(CH2)7–COOH
Provas
Questão presente nas seguintes provas
Considere os seguintes exemplos de exercício e problema.
1. Exercício – Calcule a concentração, em mol/L, de íon cloro
em uma solução formada a partir da dissolução de 2,0 g de NaCl
em 1 L de água.
2. Problema – Qual é a concentração de íons cloro na água de
torneira?
A próxima tabela ressalta aspectos que caracterizam um exercício
e um problema.

Os problemas podem ser usados para operacionalizar um conceito, treinar um algoritmo, exemplificar etc.
Provas
Questão presente nas seguintes provas
Considere os seguintes exemplos de exercício e problema.
1. Exercício – Calcule a concentração, em mol/L, de íon cloro
em uma solução formada a partir da dissolução de 2,0 g de NaCl
em 1 L de água.
2. Problema – Qual é a concentração de íons cloro na água de
torneira?
A próxima tabela ressalta aspectos que caracterizam um exercício
e um problema.

Os exercícios podem ser utilizados para desenvolver conteúdos procedimentais e atitudinais e para proporcionar a complexificação dos conceitos e o desenvolvimento de raciocínio.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container