Foram encontradas 60 questões.
Em uma aula experimental sobre eletrólise, um professor ligou
três cubas eletrolíticas (I, II e III) em série, como ilustra a figura a
seguir.
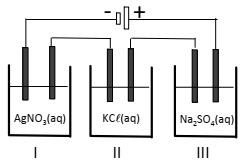
Cada cuba era constituída por um par de eletrodos inertes, continham soluções aquosas de AgNO3, KCl e Na2SO4 de mesma concentração e operaram durante um mesmo período de tempo em iguais condições.
A partir dessas informações, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Na cuba I observa-se formação de gás no cátodo.
( ) Na cuba II o pH da solução aumenta ao longo do processo. ( ) Na cuba III um depósito sólido é formado no ânodo.
As afirmativas são, respectivamente,

Cada cuba era constituída por um par de eletrodos inertes, continham soluções aquosas de AgNO3, KCl e Na2SO4 de mesma concentração e operaram durante um mesmo período de tempo em iguais condições.
A partir dessas informações, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Na cuba I observa-se formação de gás no cátodo.
( ) Na cuba II o pH da solução aumenta ao longo do processo. ( ) Na cuba III um depósito sólido é formado no ânodo.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
Estereoisômeros apresentam propriedades químicas idênticas,
mas diferem quanto à propriedade física de girar o plano de luz
polarizada. Todavia, a síntese seletiva desses compostos é
complexa e, portanto, eles são frequentemente obtidos em
laboratório na forma de misturas racêmicas.
Considere a síntese em laboratório de uma molécula quiral que produziu uma mistura racêmica contendo 12,5% de cada estereoisômero.
A molécula sintetizada foi o
Considere a síntese em laboratório de uma molécula quiral que produziu uma mistura racêmica contendo 12,5% de cada estereoisômero.
A molécula sintetizada foi o
Provas
Questão presente nas seguintes provas
O cobalto-60, utilizado no tratamento de câncer, pode ser
preparado através de um processo denominado transmutação
induzida por nêutron.
Esse processo ocorre em três etapas e inicia-se a partir do ferro58. Na primeira etapa, o ferro-58 é convertido a ferro-59 pela
absorção de um nêutron. A segunda etapa consiste no
decaimento beta do ferro-59 para cobalto-59. Na etapa final, o
cobalto-59 absorve outro nêutron, sendo convertido a cobalto-60.
A reação global do processo de transmutação descrito pode ser representada po
A reação global do processo de transmutação descrito pode ser representada po
Provas
Questão presente nas seguintes provas
O cloreto de fosforila (POCl3), usado na síntese de ésteres, pode
sofrer decomposição segundo a reação abaixo.
2 POCl3(g) → 2 PCl3(g) + O2(g)
Nas condições-padrão a 298 K, a variação de entalpia (ΔH0 ) e a variação de entropia (ΔS 0 ) para esse processo valem, respectivamente, 572 kJ e 179 J/K. A partir das informações apresentadas, analise as afirmações a seguir.
I. O processo de decomposição do cloreto de fosforila é endotérmico. II. O processo leva à diminuição da desordem do sistema. III. O processo é não-espontâneo nas condições-padrão.
Está correto apenas o que se afirma em
2 POCl3(g) → 2 PCl3(g) + O2(g)
Nas condições-padrão a 298 K, a variação de entalpia (ΔH0 ) e a variação de entropia (ΔS 0 ) para esse processo valem, respectivamente, 572 kJ e 179 J/K. A partir das informações apresentadas, analise as afirmações a seguir.
I. O processo de decomposição do cloreto de fosforila é endotérmico. II. O processo leva à diminuição da desordem do sistema. III. O processo é não-espontâneo nas condições-padrão.
Está correto apenas o que se afirma em
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Interações com Tecnologia, Sociedade e Meio Ambiente
Antes de chegar às casas para uso doméstico, a água passa por
uma série de tratamentos. Em uma das etapas desse processo
são adicionados o sulfato de alumínio e o óxido de cálcio à água.
O produto gelatinoso formado na reação entre esses compostos
arrasta para baixo as partículas suspensas na água, removendo
assim praticamente toda matéria finamente dividida.
Ao processo descrito dá-se o nome de
Provas
Questão presente nas seguintes provas
Considere um sistema em equilíbrio formado a partir da reação
entre o ácido fluorídrico e o íon oxalato, sendo Keq a constante de
equilíbrio.
2HF(aq) + C2O42-(aq) ⇆ 2F-(aq) + H2C2O4(aq) Keq
Sabe-se ainda que
(I) HF(aq) ⇆ H+ (aq) + F– (aq) K1
(II) H2C2O4 (aq) ⇆ 2H+ (aq) + C2O4 2– (aq) K2
O valor da constante de equilíbrio Keq pode ser expresso em função das constantes K1 e K2 pela expressão
2HF(aq) + C2O42-(aq) ⇆ 2F-(aq) + H2C2O4(aq) Keq
Sabe-se ainda que
(I) HF(aq) ⇆ H+ (aq) + F– (aq) K1
(II) H2C2O4 (aq) ⇆ 2H+ (aq) + C2O4 2– (aq) K2
O valor da constante de equilíbrio Keq pode ser expresso em função das constantes K1 e K2 pela expressão
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaEletroquímica
Entre os diversos óxidos de nitrogênio, o mais comum é o óxido
nítrico (NO), um gás incolor, levemente tóxico, que pode ser
preparado em laboratório pela redução do ácido nítrico diluído,
usando-se cobre como agente redutor. A equação não
balanceada do processo é apresentada a seguir.
Cu(s) + NO3 – (aq) + H+ (aq) → Cu+2(aq) + NO(g) + H2O(l)
A soma dos menores inteiros que balanceiam corretamente a equação descrita é igual a
Cu(s) + NO3 – (aq) + H+ (aq) → Cu+2(aq) + NO(g) + H2O(l)
A soma dos menores inteiros que balanceiam corretamente a equação descrita é igual a
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
O composto U 46 Br, cuja estrutura está representada a seguir, é
um herbicida usado em culturas de cana-de-açúcar. Apesar de
seus efeitos extremamente tóxicos, tem registro para uso no
Ministério da Agricultura, Pecuária e Abastecimento do Brasil.
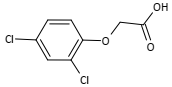
No composto U 46 BR são identificadas as funções

No composto U 46 BR são identificadas as funções
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Devido a sua elevada reatividade, o flúor é capaz de formar
compostos químicos com diversos elementos, inclusive gases
nobres. Entre eles estão ClF3, BrF5 e o XeF4.
As geometrias moleculares apresentadas por esses compostos
são, respectivamente, iguais a
Provas
Questão presente nas seguintes provas
A facilidade com que os elétrons são removidos de um átomo é
um indicador importante sobre seu comportamento químico.
Observe o gráfico a seguir, que contém a variação de energia
para as sucessivas ionizações de um elemento químico X.
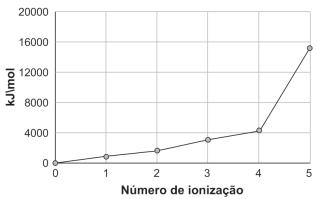
De acordo com as informações, o elemento X é o

De acordo com as informações, o elemento X é o
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container