Foram encontradas 60 questões.
Leia o trecho, da música do Emicida (Passarinhos) com a participação da Vanessa da Mata.
"No pé que as coisas vão, jão
Doidera, daqui a pouco, resta madeira nem pro caixão
Era neblina, hoje é poluição
Asfalto quente queima os pés no chão
Carros em profusão, confusão
Água em escassez, bem na nossa vez
Assim não resta nem as barata Injustos fazem leis e o que resta pro ceis?
Escolher qual veneno te mata". Passarinhos,
Emicida e Vanessa da Mata.
Neste trecho da música do Emicida, a preocupação com o uso dos recursos naturais é notória. E nos faz refletir sobre as questões ambientais e suas implicações tecnológicas, sociais e científicas que fazem parte da nossa vida pessoal e profissional. Sendo assim, assinale a alternativa que apresenta quais problemáticas ambientais podemos relacionar ao trecho da música Passarinhos, de Emicida.
Provas
O processo mais usado para a obtenção do alumínio metálico é o Processo de Hall-Héroult. O alumínio é fundido verticalmente de modo semi contínuo produzindo lingotes de alumínio, folhas de alumínio ou blocos de alumínio, utilizados diretamente em produtos semiacabados. O resfriamento das peças de alumínio é acelerado por jatos de água. Os lingotes retangulares grandes, que podem pesar até 25 toneladas passam por uma espiral quente levando, posteriormente, à fabricação de produtos como o papel alumínio. De 4 a 5 toneladas de Bauxita (minério), são produzidas 2 toneladas de alumina (Al2O3), que, por sua vez, produzem 1 tonelada de alumínio (Al). Apesar de a performance na produção de alumínio não sofrer grandes mudanças de acordo com a usina, a quantidade final pode variar de acordo com a capacidade de processamento da usina de produção de alumínio, enquanto algumas produzem 200 toneladas por ano, outras podem produzir cerca de 400 mil toneladas/ano.
Adaptado.Produção de Alumínio: Extração da Bauxita, Obtenção na Eletrólise (culturalivre.com). (Acesso em 24 de Julho de 2021).
Podemos resumir a reação de obtenção do alumínio a partir do óxido de alumínio por meio da seguinte equação química balanceada.
!$ 2\,\,Al_2 O_3 (I) + 3 C(s) \rightarrow 4 Al(I) + 3 CO_2(g) !$
Dados: Massas atômicas (g/mol) Al=27; C=12; O=16.
Assinale a alternativa que apresenta a massa, em gramas, de alumínio produzida se tivermos o triplo da quantidade, em mol, de óxido de alumínio e carvão.
Provas
O cobre é um metal com alta durabilidade, resistência à corrosão, maleabilidade e ductilidade. Por isso, pode ser transformado em fios, lâminas, bastões etc. Alguns processos de obtenção do cobre metálico, envolvem uma série de etapas com o minério extraído, britado e moído até a obtenção do metal isolado. Um dos minérios de cobre é a calcosita (Cu2S), que tem em sua composição sulfetos (compostos de enxofre). Por isso, é aquecida na presença de gás oxigênio (O2), que reage com o enxofre, formando o dióxido de enxofre (SO2) e liberando o cobre na forma simples (Cu). Esse processo recebe o nome de ustulação. Ele é representado pela equação química não balanceada a seguir:
!$ Cu_2S(s) + O_2(g) \rightarrow Cu(s) + SO_2 (g) !$
Dados: Massas atômicas (g/mol): Cu= 63,5; S=32; O=16.
Assinale a alternativa que apresenta qual será a massa aproximada em toneladas de cobre metálico produzido, se tivermos 20 toneladas do minério de cobre (Cu2S) com pureza de 80% e gás oxigênio suficiente.
Provas
A pilha de lítio é usada em marca-passos implantados no interior da caixa torácica do paciente para controlar as batidas do coração por meio de impulso. Essa pilha é bastante leve, pesando apenas 25 g. Foi desenvolvida principalmente para ser utilizada em marca-passos, pois além de ter uma grande durabilidade (que pode chegar a até 10 anos), ela não solta gases que poderiam ser prejudiciais ao paciente, sendo fechada hermeticamente. Sua voltagem também é grande, variando de 2,8 V a 3,4 V. Sua constituição básica tem lítio metálico no ânodo e um complexo de iodo ou uma mistura de soluções, como por exemplo, o cloreto de sulfurila (SOCl2) no cátodo. Esses dois eletrodos sólidos são separados por uma camada cristalina de iodeto de lítio, por onde a corrente elétrica passa do ânodo para o cátodo.
Adaptado. Pilhas e Baterias de Lítio. Pilha e Baterias de íon lítio (uol.com.br). (Acesso em 23 de Julho de 2021).
Com relação à pilha de lítio usada em marca-passos e as transformações nela ocorridas, assinale a alternativa correta.
Provas
A maior parte dos tipos de bafômetros utilizados pela polícia federal funcionam a base de reações químicas. O dicromato de potássio e a célula de combustível são os principais reagentes. Em ambos os testes, o motorista deve assoprar no bafômetro com força (sopro de 5 segundos). Assim, o bafômetro (dicromato de potássio) funciona da seguinte maneira:
- O ar expelido pelos pulmões do suspeito é bombeado em uma solução de dicromato de potássio fortemente acidulada (ácido sulfúrico); - O etanol presente na boca do motorista (se este consumiu bebida alcoólica) reage com os íons dicromato da solução, produzindo acetaldeído e íons Cromo (III); - Em razão da reação química, ocorre uma mudança na cor da solução, a cor característica laranja passa para um tom esverdeado, acusando a presença de álcool etílico ou etanol.
Adaptado. Composição química do Bafômetro - Mundo Educação (uol.com.br). (Acesso em 23 de Julho de 2021)
A reação que ocorre no bafômetro com dicromato de potássio está representada pela equação química não balanceada a seguir:
!$ { \underset{ alaranjado} {K_2 Cr_2 O_{7(aq)}}} + x H_2 SO_{4(aq)} { \underset{ incolor} {3 C H_3}} CH_2 OH_{ (g) \rightarrow} { \underset{ verde} { Cr_2(SO_4)}} = y { \underset{ incolor} {H_2 O_{(I)} + 3}} C H_3 CHO_{(g)} + K_2 SO_{4(aq)} !$
Assinale a alternativa que relaciona a classificação e os respectivos valores de x e y (mínimos coeficientes inteiros) que balanceiam corretamente a reação do bafômetro com dicromato de potássio.
Provas
Observe a tabela a seguir. Nela estão algumas substâncias químicas e suas principais aplicações nas atividades industriais e até mesmo do nosso cotidiano.
| Substâncias químicas | Aplicações |
| Ácido Fosfórico | Indústrias de vidro, de alimentos, na tinturaria e na fabricação de fosfatos e superfosfatos usados como adubos (fertilizantes); acidulante em refrigerantes e gomas de mascar. |
| Óxido de Cálcio | Cal virgem. Usado na construção civil e no controle de pH de solos (calagem) |
| Hidróxido de Alumínio | Antiácido estomacal. Suas nanopartículas podem atuar como suportes catalíticos; isto é, o catalisador se liga a eles para permanecer fixo em sua superfície, onde as reações químicas são aceleradas. |
| Hipoclorito de Sódio | Substância muito utilizada como desinfetante para superfícies, mas que também pode ser utilizada para purificar a água para uso e consumo humano. Em solução ele é conhecido popularmente como água sanitária ou cândida. |
Assinale a alternativa que apresenta as fórmulas químicas que representam as substâncias presentes na tabela acima.
Provas
A maioria dos solos brasileiros onde se cultiva a batata é ácido, ou seja, apresenta pH abaixo da faixa ideal de cultivo (entre 5,5 e 6,0). A calagem promove importante modificação no ambiente radicular, pois diminui a acidez do solo, fornece íons Ca+2 e Mg+2, aumentando a disponibilidade e a eficiência na utilização de vários nutrientes. Assim, apesar de ser considerada relativamente tolerante à acidez do solo, a cultura da batata responde positivamente à aplicação de corretivos da acidez. Neste contexto, a quantidade de corretivo deve ser determinada com base na análise química e física do solo, no poder relativo de neutralização total (PRNT) do corretivo e na profundidade de incorporação. Recomenda-se muito cuidado no cálculo da calagem, pois calcário em excesso eleva o pH acima de 6,0, favorecendo o ataque da sarna-comum, uma das doenças de maior dificuldade de controle na cultura da batata.
Adaptado.https://www.embrapa.br/documents/1355126/49258452/embrapa.br-Corre%C3%A7%C3%A3o+do+Solo+-+Portal+Embrapa.pdf/8a01a49d-0b94-c4e4-ea38-5682ceb37955. (Acesso em 23 de Julho de 2021). O processo de calagem do solo citado
O processo de calagem do solo citado anteriormente no texto refere-se à utilização de calcário (CaCO3) para diminuir a acidez dos solos. Assim, quando o carbonato de cálcio é adicionado ao solo, ele pode reagir de vários modos. Assinale a alternativa que apresenta as equações químicas que podem ocorrer neste processo.
Provas
A geometria molecular de moléculas e de íons considera que os pares eletrônicos da camada de valência são arranjados ao redor de cada átomo, deixando-os o mais afastado possível, minimizando assim a repulsão eletrônica. Ainda, devemos lembrar que nem sempre a geometria molecular é exatamente aquela prevista pelos domínios eletrônicos e que os pares não ligados não fazem parte da geometria molecular: somente os átomos ligados devem ser contabilizados.
Adaptado. Chapter 9 Molecular
Geometries and Bonding Theories (ufpr.br). (Acesso em 23 de Julho de 2021).
Observe a tabela a seguir. E assinale a alternativa que apresenta a sequência que relaciona corretamente a substância ou o íon à sua geometria molecular, respectivamente.
| Substâncias/íons | Geometria Molecular |
| I. NH3 | ( ) Angular |
| II. PH4+ | ( ) Linear |
| III. H2O | ( ) Tetraédrica |
| IV. CO2 | ( ) Piramidal |
Dados: Números atômicos (Z) H = 1; C = 6; N = 7; O = 8; P =15.
Provas
O etanol ou álcool etílico é solúvel em água em qualquer proporção, pois apresenta infinita solubilidade em água. Já a gasolina apresenta baixa solubilidade em água. Sabemos que um dos princípios importantes na dissolução de solutos é que “materiais semelhantes se dissolvem”. Observe as fórmulas estruturais do etanol e da água a seguir:
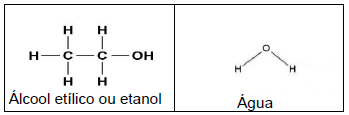
Após observar as fórmulas estruturais do etanol e da água, reconhecemos que o etanol se dissolve em água devido à formação de :
Assinale a alternativa que preencha corretamente a lacuna.
Provas
A Tabela Periódica é uma listagem que agrupa todos os elementos químicos conhecidos. Trata-se de um instrumento relevante para a Química, pois contém uma enorme quantidade de informações sobre todos os elementos químicos, como seus estados físicos, suas propriedades físicas e químicas, suas massas e números atômicos etc. Os elementos encontram-se organizados em ordem crescente de seus números atômicos (número de prótons).
Observe a tabela a seguir que apresenta alguns elementos químicos genericamente identificados pelos números I, II, III, IV e V, com sua respectiva distribuição eletrônica.
| Elementos Químicos | Distribuição Eletrônica |
| I | 1s2 2s2 2p6 3s23p3 |
| II | 1s2 2s2 2p6 3s2 3p6 4s2 3d8 |
| III | 1s2 2s2 2p6 3s2 3p6 4s2 |
| IV | 1s2 2s2 2p6 3s2 3p6 4s23d10 4p3 |
| V | 1s2 2s2 2p6 3s2 3p6 |
De acordo com as informações localizadas na tabela acima, é correto afirmar que:
Provas
Caderno Container