Os gráficos a seguir mostram resultados obtidos após a aplicação do método dos mínimos quadrados em estudos cinéticos a respeito da reação \(2\,N_2\,O_{5\,\mathrm\,(g)}\,\rightarrow\,4\,NO_{2\,\mathrm\,{(g)}}\,+\,O_{2\,\mathrm\,{(g)}}\).
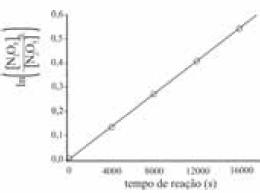
Gráfico 1. Gráfico do logaritmo natural da razão entre a concentração inicial do N2O5(g) − ([N2O5]0) − e sua concentração − [N2O5] − em função do tempo de reação a 25 ºC.
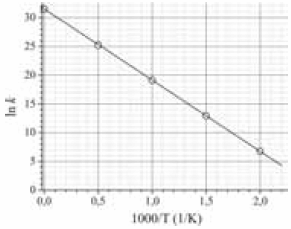
Gráfico 2. Gráfico do logaritmo natural da constante de velocidade, k, em função do inverso da temperatura absoluta, T, multiplicado por 1.000.
Considerando as informações fornecidas e que a constante dos gases ideais seja igual a 8,3 J.mol-1.K-1, julgue o próximo item.
A reação em questão apresenta cinética de segunda ordem.