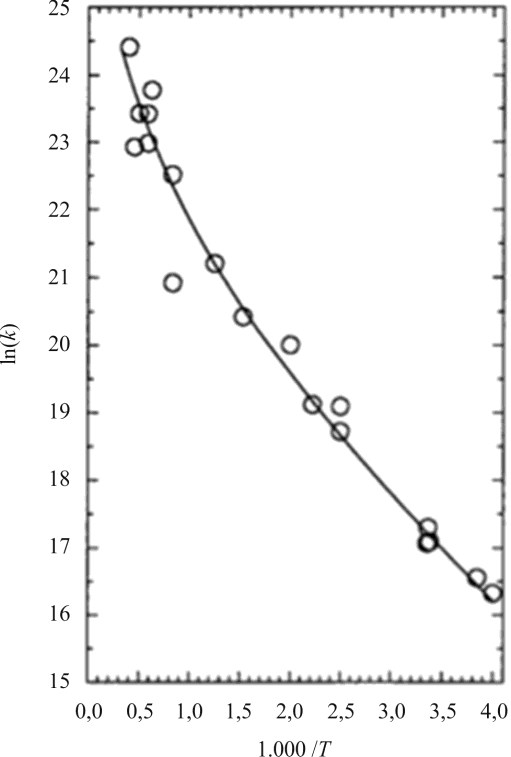
J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Nos resultados experimentais apresentados no gráfico, a constante de velocidade k obedece à lei usual de Arrhenius em toda a faixa de temperaturas do experimento.