Foram encontradas 240 questões.
A imunoterapia, um dos tratamentos mais utilizados contra o câncer, consiste em empregar células imunológicas do próprio paciente para atacar e destruir os tumores. Utilizam-se os linfócitos T, que, infiltrados nos tumores, atacam suas células. Com relação a esse assunto e ao sistema imunológico, julgue os itens a seguir.
A imunoterapia teria o mesmo sucesso caso fossem utilizados linfócitos de outro indivíduo, uma vez que a resposta imunitária no tecido afetado seria a mesma.
Provas
O gás dióxido de enxofre é um dos principais poluentes atmosféricos que afetam a vida do homem. Para quantificá-lo na atmosfera, o analista químico, inicialmente, monta um sistema para coletar o dióxido de enxofre, utilizando um borbulhador, isto é, um frasco contendo solução de peróxido de hidrogênio, onde o ar atmosférico é borbulhado com o auxílio de uma bomba que o aspira. A figura a seguir representa um tipo de borbulhador e dispositivos usados na coleta da amostra de ar a ser analisada. No cálculo da concentração do gás em estudo, é importante medir o volume de ar da amostra por meio de um totalizador de volume que mede todo o ar que passou pelo borbulhador. Finalizada a amostragem, o analista químico determina a quantidade de ácido sulfúrico formado no borbulhador, titulando-o com solução de base forte NaOH, por exemplo, e calcula a quantidade proporcional de dióxido de enxofre. Utilizando-se o volume total do ar amostrado, é possível, então, calcular a concentração de dióxido de enxofre na amostra de ar.
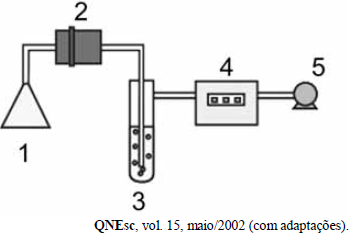
Sistema para dosagem do SO2: 1– entrada de ar em forma de funil; 2 – filtro para retenção das partículas; 3 – borbulhador contendo solução de água oxigenada; 4 – totalizador de volume para medida do ar total amostrado; 5 – bomba para aspirar o ar.
Considere que a seguinte reação ocorra no borbulhador.
SO2(g) + H2O2(l) → H2SO4(aq)
Com base nas informações acima, julgue os itens de 101 a 104.
Com base na equação da reação química que ocorre no borbulhador, é correto afirmar que o peróxido de hidrogênio atuou no processo como agente oxidante.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O gás dióxido de enxofre é um dos principais poluentes atmosféricos que afetam a vida do homem. Para quantificá-lo na atmosfera, o analista químico, inicialmente, monta um sistema para coletar o dióxido de enxofre, utilizando um borbulhador, isto é, um frasco contendo solução de peróxido de hidrogênio, onde o ar atmosférico é borbulhado com o auxílio de uma bomba que o aspira. A figura a seguir representa um tipo de borbulhador e dispositivos usados na coleta da amostra de ar a ser analisada. No cálculo da concentração do gás em estudo, é importante medir o volume de ar da amostra por meio de um totalizador de volume que mede todo o ar que passou pelo borbulhador. Finalizada a amostragem, o analista químico determina a quantidade de ácido sulfúrico formado no borbulhador, titulando-o com solução de base forte NaOH, por exemplo, e calcula a quantidade proporcional de dióxido de enxofre. Utilizando-se o volume total do ar amostrado, é possível, então, calcular a concentração de dióxido de enxofre na amostra de ar.

Sistema para dosagem do SO2: 1– entrada de ar em forma de funil; 2 – filtro para retenção das partículas; 3 – borbulhador contendo solução de água oxigenada; 4 – totalizador de volume para medida do ar total amostrado; 5 – bomba para aspirar o ar.
Considere que a seguinte reação ocorra no borbulhador.
SO2(g) + H2O2(l) → H2SO4(aq)
Com base nas informações acima, julgue os itens de 101 a 104.
Considerando que, na titulação do ácido sulfúrico formado no borbulhador, foram gastos 3,2 mol de NaOH e que o totalizador de volume indicou 4 m3 de amostra de ar, conclui-se que, nessa análise, a concentração de dióxido de enxofre no ar amostrado era de 8 × 10-4 mol / L.
Provas
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Química InorgânicaMateriais homogêneos e heterogêneos. Separação de misturas.
O gás dióxido de enxofre é um dos principais poluentes atmosféricos que afetam a vida do homem. Para quantificá-lo na atmosfera, o analista químico, inicialmente, monta um sistema para coletar o dióxido de enxofre, utilizando um borbulhador, isto é, um frasco contendo solução de peróxido de hidrogênio, onde o ar atmosférico é borbulhado com o auxílio de uma bomba que o aspira. A figura a seguir representa um tipo de borbulhador e dispositivos usados na coleta da amostra de ar a ser analisada. No cálculo da concentração do gás em estudo, é importante medir o volume de ar da amostra por meio de um totalizador de volume que mede todo o ar que passou pelo borbulhador. Finalizada a amostragem, o analista químico determina a quantidade de ácido sulfúrico formado no borbulhador, titulando-o com solução de base forte NaOH, por exemplo, e calcula a quantidade proporcional de dióxido de enxofre. Utilizando-se o volume total do ar amostrado, é possível, então, calcular a concentração de dióxido de enxofre na amostra de ar.

Sistema para dosagem do SO2: 1– entrada de ar em forma de funil; 2 – filtro para retenção das partículas; 3 – borbulhador contendo solução de água oxigenada; 4 – totalizador de volume para medida do ar total amostrado; 5 – bomba para aspirar o ar.
Considere que a seguinte reação ocorra no borbulhador.
SO2(g) + H2O2(l) → H2SO4(aq)
Com base nas informações acima, julgue os itens de 101 a 104.
O método de separação de misturas representado pelo dispositivo 2, representado na figura, também é eficaz para a separação dos componentes da solução resultante do processo de titulação empregado na dosagem do ácido sulfúrico.
Provas
O gás dióxido de enxofre é um dos principais poluentes atmosféricos que afetam a vida do homem. Para quantificá-lo na atmosfera, o analista químico, inicialmente, monta um sistema para coletar o dióxido de enxofre, utilizando um borbulhador, isto é, um frasco contendo solução de peróxido de hidrogênio, onde o ar atmosférico é borbulhado com o auxílio de uma bomba que o aspira. A figura a seguir representa um tipo de borbulhador e dispositivos usados na coleta da amostra de ar a ser analisada. No cálculo da concentração do gás em estudo, é importante medir o volume de ar da amostra por meio de um totalizador de volume que mede todo o ar que passou pelo borbulhador. Finalizada a amostragem, o analista químico determina a quantidade de ácido sulfúrico formado no borbulhador, titulando-o com solução de base forte NaOH, por exemplo, e calcula a quantidade proporcional de dióxido de enxofre. Utilizando-se o volume total do ar amostrado, é possível, então, calcular a concentração de dióxido de enxofre na amostra de ar.

Sistema para dosagem do SO2: 1– entrada de ar em forma de funil; 2 – filtro para retenção das partículas; 3 – borbulhador contendo solução de água oxigenada; 4 – totalizador de volume para medida do ar total amostrado; 5 – bomba para aspirar o ar.
Considere que a seguinte reação ocorra no borbulhador.
SO2(g) + H2O2(l) → H2SO4(aq)
Com base nas informações acima, julgue os itens de 101 a 104.
O dióxido de enxofre, além ser um poluente atmosférico associado à formação de precipitações ácidas, tem destacado papel como gás estufa, influindo no aquecimento global.
Provas
O chamado pó químico, que é utilizado em muitos extintores de incêndio, é uma mistura de bicarbonato de sódio, bicarbonato de potássio e aditivos, como o bórax (Na2B4O7A10H2O). Em altas temperaturas, a degradação do bicarbonato de sódio ocorre conforme a equação a seguir.
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l).
As substâncias produzidas não são nem combustíveis nem comburentes, portanto são capazes de extinguir o fogo.
F. de Farias. Introdução à química forense. Campinas: Átomo, 2007 (com adaptações).
Com relação ao assunto acima abordado, julgue os itens a seguir.
Da análise da estrutura do dióxido de carbono (CO2), conclui-se que, apesar de a ligação entre C e O ser polar, a molécula é apolar pelo fato de sua geometria ser linear.
Provas
O chamado pó químico, que é utilizado em muitos extintores de incêndio, é uma mistura de bicarbonato de sódio, bicarbonato de potássio e aditivos, como o bórax (Na2B4O7A10H2O). Em altas temperaturas, a degradação do bicarbonato de sódio ocorre conforme a equação a seguir.
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l).
As substâncias produzidas não são nem combustíveis nem comburentes, portanto são capazes de extinguir o fogo.
F. de Farias. Introdução à química forense. Campinas: Átomo, 2007 (com adaptações).
Com relação ao assunto acima abordado, julgue os itens a seguir.
O raio do íon sódio (Na+) é inferior ao do íon potássio (K+).
Provas
O chamado pó químico, que é utilizado em muitos extintores de incêndio, é uma mistura de bicarbonato de sódio, bicarbonato de potássio e aditivos, como o bórax (Na2B4O7A10H2O). Em altas temperaturas, a degradação do bicarbonato de sódio ocorre conforme a equação a seguir.
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l).
As substâncias produzidas não são nem combustíveis nem comburentes, portanto são capazes de extinguir o fogo.
F. de Farias. Introdução à química forense. Campinas: Átomo, 2007 (com adaptações).
Com relação ao assunto acima abordado, julgue os itens a seguir.
O fato de o carbono na molécula de CO2 apresentar estado de oxidação o mais reduzido possível corrobora a informação mencionada no texto de que essa substância não atua como combustível.
Provas
O chamado pó químico, que é utilizado em muitos extintores de incêndio, é uma mistura de bicarbonato de sódio, bicarbonato de potássio e aditivos, como o bórax (Na2B4O7A10H2O). Em altas temperaturas, a degradação do bicarbonato de sódio ocorre conforme a equação a seguir.
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l).
As substâncias produzidas não são nem combustíveis nem comburentes, portanto são capazes de extinguir o fogo.
F. de Farias. Introdução à química forense. Campinas: Átomo, 2007 (com adaptações).
Com relação ao assunto acima abordado, julgue os itens a seguir.
O bicarbonato de sódio é um hidrogenossal que apresenta, em sua estrutura, ligações iônicas e covalentes.
Provas
Entre os ingredientes presentes na composição de bebidas refrigerantes de baixa caloria, denominadas diet ou light, estão os conservantes e os edulcorantes. Um desses conservantes, o ácido benzoico, atua contra praticamente todas as espécies de micro-organismos, evitando deteriorações causadas por leveduras, mofos e bactérias. Por ser pouco solúvel em água, esse ácido é utilizado na forma de benzoato de sódio. No Brasil, o teor máximo permitido desse conservante é de 500 mg de ácido benzoico por 100 mL de refrigerante. Dos edulcorantes, o mais empregado é o aspartame, cujo poder adoçante é 200 vezes maior que o do açúcar comum de sacarose.
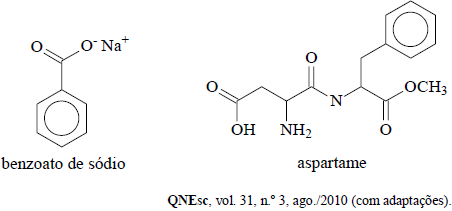
Com base nas informações acima, julgue os itens a seguir.
Considerando-se que o aspartame se degrada em aspartilfenilalanina e metanol sob exposição prolongada ao calor, de acordo com a equação química a seguir, é correto afirmar que, nessas condições, a molécula de aspartame sofre oxidação.
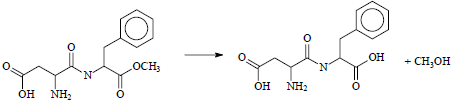
Provas
Caderno Container