Foram encontradas 60 questões.
Uma maneira bastante simples de calcular a velocidade que um fluido irá atingir ao percorrer uma tubulação é utilizando a equação de Bernoulli. Essa equação é uma forma simplificada de expressar o balanço de energia de um sistema, em que são consideradas somente as energias potencial gravitacional, pressão e cinética.
!$ \left ( h\,\,g + { \Large { P \over p}} + { \Large { v^2 \over 2}} \right) = constante\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,Equação\,de\,Bernoulli !$
Fonte: HOLLAND, F. A.; BRAGG, R. Fluid Flow for Chemical Engineers. 2 ed. Londres: Arnold, 1995. p. 16.
Como a equação apresentada não contempla perda de carga, há uma diferença entre os valores de velocidade real e a calculada por essa equação, sendo a velocidade real sempre menor do que a calculada. Complete a frase: A partir de uma mesma velocidade de entrada na tubulação, haverá um aumento na diferença entre a velocidade calculada pela equação de Bernoulli apresentada e a real ao se
Provas
Leia o texto a seguir.
Naquele momento da reunião, ponderei:
“Sou eu mesma. E você eu conheço do Centro de Instruções, certo?”
Ela me olhou interrogativa (forcejando para ser alegre).
Fonte: Arquivo da Banca Elaboradora.
Além da estrutura sintática, a pontuação indica vários outros aspectos presentes no texto e que podem ser assim explicados e exemplificados:
I. Os parênteses exemplificam uma indicação cênica.
II. As aspas ressaltam o valor significativo das frases.
III. A vírgula, na primeira frase, está isolando um adjunto adverbial.
IV. A vírgula antes de “certo?” isola uma expressão de caráter fático.
V. Os dois pontos indicam que o sentido vai além do que foi expresso.
Está correto apenas o que se afirma em
Provas
Provas
Em um laboratório e ;rio havia 3 compostos orgânicos identificadas como I, II e III. Sob determinadas condições, observou-se que:
• As substâncias I e II reagem formando uma amida.
• As substâncias II e III reagem formando um éster.
• A substância III, caso mantida em um meio oxidativo e ácido, pode se transformar em II.
As substâncias I, II e III são, nessa ordem,
Provas
Uma das ferramentas que pode auxiliar nos estudos de obtenção de tampões ou até mesmo de precipitação, é o digrama de especiação. Nesse diagrama, podem ser observadas as espécies presentes no meio para diferentes valores de pH e suas concentrações (representadas como pC, que é o negativo do logaritmo das concentrações). A seguir, está apresentado o diagrama de especiação do ácido cianídrico, a 25°C para uma concentração total de cianeto igual a 10-3mol/L (pC=3). O ácido cianídrico é altamente tóxico, no entanto é largamente utilizado no tratamento de ouro.
Diagrama de especiação para o ácido cianídrico a 25°C
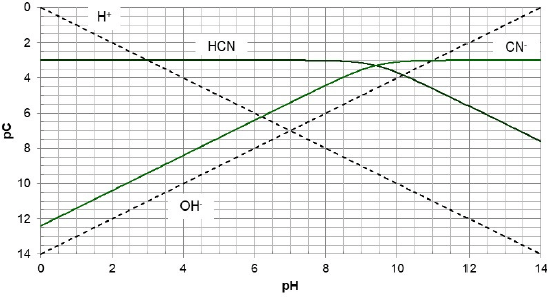
Fonte: Arquivo da Banca Elaboradora.
A partir do diagrama, considerando que uma solução com concentração de 10-3mol/L de ácido cianídrico seja ideal, a 25°C, em um recipiente fechado, o pH da solução será igual a
Provas
Em um reator foram colocados 50mol de uma substância A e 50mol de uma substância B. Essas substâncias reagem segundo as equações.
!$ A + B \rightleftarrows C\\A + C \rightleftarrows D !$
Quando o sistema atinge o equilíbrio, as frações molares de A e B são 0,05 e 0,10, respectivamente. Já as frações de C e D são:
Provas
Provas
Provas
A seguir são apresentadas as entalpias de formação de alguns compostos. Analise-as
| Composto | Fórmula | ΔHformação (kJ/mol) |
| Metano (g) | CH4 | -74,5 |
| Etano (g) | C2H6 | -83,8 |
| Propano (g) | C3H8 | -104,7 |
| n-Butano (g) | C4H10 | -125,8 |
| n-Octano (g) | C8H18 | -208,8 |
| Etileno (g) | C2H4 | 52,5 |
| Etanol (g) | C2H6O | -235,1 |
| Água (g) | H2O | -393,5 |
| Dióxido de carbono (g) | CO2 | -241,8 |
SMITH, J. M.; VAN NESS, H. C.; ABBOTT, M. M.
Introdução à termodinâmica da Engenharia Química. 7 ed. Rio de Janeiro: LTC, 2007. p. 514-515.
A partir da análise desses dados, é correto afirmar que
Provas
Um vaso fechado, a 1 20°C, contém 0,55mol de fenol e 0,45mol de tolueno. Nessa temperatura, a pressão de vapor do fenol é 13,0kPa e a do metanol é 131,3kPa. Considerando que o sistema se encontra no ponto de orvalho, que a fase líquida se comporta como uma solução ideal e a fase vapor se comporta como uma mistura de gases ideais, a pressão no interior do vaso é
Provas
Caderno Container