Foram encontradas 60 questões.
A mistura entre íons permanganato e peróxido, em meio ácido, pode ser representada pela seguinte equação não balanceada:
MnO4 –(aq) + H2O2(aq) + H+(aq) → Mn2+(aq) + O2(g) + H2O(!$ \ell !$)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2O2; E0 = + 0,68 V
MnO4 –(aq) + 8 H+(aq) + 5 e– → Mn2+(aq) + 4 H2O(!$ \ell !$); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
Provas
No mecanismo que mostra a reação de desidratação de um álcool, os asteriscos nos intermediários 1 e 2 indicam ligações incompletas dos respectivos átomos de carbono.
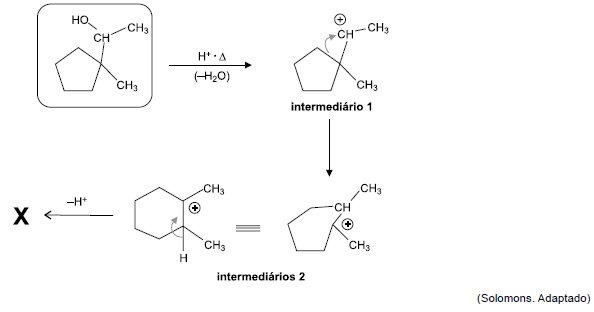
A estrutura de X que representa o produto principal da reação é:
Provas
A 100 mL de uma solução contendo 1×10–2 mol.L–1 em íons Mg2+ foram adicionados 100 mL de hidróxido de sódio 0,10 mol.L–1 precipitando Mg(OH)2 (kps, a 25 ºC = 9×10–12). A concentração de íons Mg2+ em solução, após a reação é de
Provas
A pirâmide olfativa usada na formulação de perfumes considera a volatilidade das substâncias.
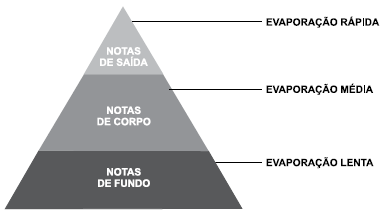
(O que significa no perfume as notas de saída, corpo e fundo? Moda Masculina Journal. Adaptado)
tabela reúne a pressão de vapor de algumas substâncias a 25 ºC e respectivos aromas.
|
Substância |
Aroma |
Pressão de vapor |
| I |
rosa |
0,02000 mmHg |
| II | coco |
0,009000 mmHg |
| III | tangerina |
0,5320 mmHg |
De acordo com as informações fornecidas, pode-se concluir que é nota de saída, de corpo e de fundo, respectivamente,
Provas
A reação do permanganato de potássio com glicerina é usada para demonstração de reação exotérmica e sua equação está representada a seguir:
14 KMnO4 + 4 C3H5(OH)3 → 7 K2CO3 + 7 Mn2O3 + 5 CO2 + 16 H2O
O agente oxidante e a variação do número de oxidação do elemento manganês nessa reação são, respectivamente,
Provas
O sulfeto de hidrogênio é naturalmente oxidado pelo oxigênio do ar, conforme a reação representada a seguir:
2 H2S(g) + 3 O2(g) → 2 SO2(g) + 2 H2O(g)
A tabela reúne as entalpias de formação dos componentes da reação.
|
Substância |
Entalpia de formação (kJ.mol–1) |
|
H2S(g) |
–20 |
|
H2O(g) |
–297 |
|
H2O(g) |
–242 |
Portanto, a entalpia da reação, em kJ.mol–1 de H2S(g), é, aproximadamente,
Provas
Considere as situações a seguir relativas à alteração da rapidez de reações.
I. Amaciamento de carne pela adição de papaína
II. Conservação de frutas em geladeira.
III. Antiácido efervescente em pó colocado na água.
Os fatores que alteram a rapidez das reações nas situações I, II e III são, respectivamente,
Provas
Considere a reação a seguir:
2 NO + 2 H2 → N2 + 2 H2O
A lei da velocidade para a reação é de segunda ordem para o NO e de primeira ordem para o H2. Portanto, ao dobrar a concentração de NO mantendo-se a concentração de H2, a velocidade da reação é:
Provas
A informação a seguir se refere a questão abaixo:
A maior parte da produção industrial do magnésio é obtida a partir da água do mar, onde o elemento químico magnésio se encontra na forma de íons Mg2+(aq), em concentração média de 1,3 g.L–1. O processo segue as seguintes etapas:
I. Precipitação de Mg(OH)2 por adição de cal viva.
II. Conversão a MgC!$ \ell !$2 por adição de HC!$ \ell !$.
III. Eletrólise ígnea do MgC!$ \ell !$2.
Sabendo que a constante de Faraday é 9,65×104 C.mol–1, a quantidade de carga elétrica necessária para obter todo o magnésio contido em 1 m3 de água do mar é de, aproximadamente,
Provas
Considere a estrutura a seguir:
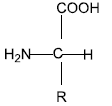
A estrutura química representada é a fórmula geral dos . A formação de cadeia polimérica dessas estruturas se dá por , formando um .
As lacunas são preenchidas, correta e respectivamente, por:
Provas
Caderno Container