Foram encontradas 120 questões.
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
A diferença entre a espectrometria de absorção atômica (AAS) e a espectrometria de emissão atômica por plasma acoplado indutivamente (ICP-AES) é que a AAS é capaz de quantificar a maioria dos ânions e dos metais, enquanto a ICP-AES é inapropriada para dosagem de ânions.
A diferença entre a espectrometria de absorção atômica (AAS) e a espectrometria de emissão atômica por plasma acoplado indutivamente (ICP-AES) é que a AAS é capaz de quantificar a maioria dos ânions e dos metais, enquanto a ICP-AES é inapropriada para dosagem de ânions.
Provas
Questão presente nas seguintes provas
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
Considerando-se o gráfico I, que mostra a curva de calibração obtida a partir da leitura da absorbância de determinado analito a 350 nm em diferentes concentrações, e o gráfico II, que ilustra o espectro obtido para uma amostra desse analito nas mesmas condições experimentais usadas para a construção da curva de calibração, é correto afirmar que a concentração do analito na amostra é maior que 15 mg/L.
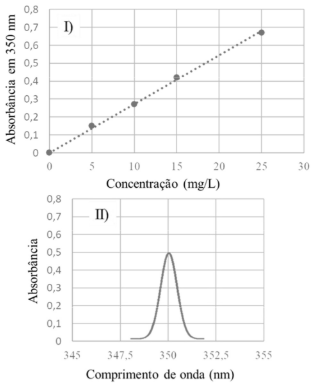
Considerando-se o gráfico I, que mostra a curva de calibração obtida a partir da leitura da absorbância de determinado analito a 350 nm em diferentes concentrações, e o gráfico II, que ilustra o espectro obtido para uma amostra desse analito nas mesmas condições experimentais usadas para a construção da curva de calibração, é correto afirmar que a concentração do analito na amostra é maior que 15 mg/L.

Provas
Questão presente nas seguintes provas
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
Situação hipotética: A absortividade molar de um analito é igual a 500,0 mol • cm−1 • L−1 quando medida a uma concentração igual a 1,0 × 10−3 mol/L em um espectofotômetro de absorção no ultravioleta visível, em determinado comprimento de onda. Assertiva: Nas mesmas condições experimentais, para que a absorbância seja igual a 0,4, o caminho óptico da cubeta contendo o analito deverá ser maior que 1,0 cm.
Situação hipotética: A absortividade molar de um analito é igual a 500,0 mol • cm−1 • L−1 quando medida a uma concentração igual a 1,0 × 10−3 mol/L em um espectofotômetro de absorção no ultravioleta visível, em determinado comprimento de onda. Assertiva: Nas mesmas condições experimentais, para que a absorbância seja igual a 0,4, o caminho óptico da cubeta contendo o analito deverá ser maior que 1,0 cm.
Provas
Questão presente nas seguintes provas
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
O esquema a seguir representa corretamente a montagem de um fotômetro de chama.
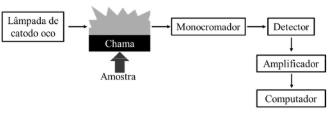
O esquema a seguir representa corretamente a montagem de um fotômetro de chama.

Provas
Questão presente nas seguintes provas
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
Para a identificação do ácido caproico, cuja estrutura molecular está representada a seguir, a espectrometria de absorção molecular no infravermelho é mais adequada que a espectrometria de absorção molecular no ultravioleta visível.
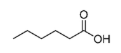
Provas
Questão presente nas seguintes provas
No que se refere a conceitos básicos em espectrofotometria, fotometria e colorimetria, julgue o item subsequente.
A absorbância de uma amostra é definida como o inverso da fração de luz que passa por essa amostra.
A absorbância de uma amostra é definida como o inverso da fração de luz que passa por essa amostra.
Provas
Questão presente nas seguintes provas
No que se refere a conceitos básicos em espectrofotometria, fotometria e colorimetria, julgue o item subsequente.
Quanto maior for a inclinação da curva de calibração, dentro da faixa dinâmica linear, maior será o limite de quantificação (LOQ) de um método.
Quanto maior for a inclinação da curva de calibração, dentro da faixa dinâmica linear, maior será o limite de quantificação (LOQ) de um método.
Provas
Questão presente nas seguintes provas
No que se refere a conceitos básicos em espectrofotometria,
fotometria e colorimetria, julgue o item subsequente.
Em um fotômetro usado para medidas colorimétricas, um filtro é usado após a cubeta, para maximizar a luz absorvida pela amostra.
Em um fotômetro usado para medidas colorimétricas, um filtro é usado após a cubeta, para maximizar a luz absorvida pela amostra.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Transformações Químicas e EnergiaEletroquímica
No que concerne a volumetria, gravimetria e potenciometria, julgue o item a seguir.
Na titulação representada pela equação seguinte, o potencial no ponto de equivalência é igual à média aritmética dos potenciais padrão de redução dos dois pares redox envolvidos na reação.
U4+ + 2 Ce4+ + 2 H2O ⇌ UO2 2+ + 2 Ce3+ + 4 H+
Na titulação representada pela equação seguinte, o potencial no ponto de equivalência é igual à média aritmética dos potenciais padrão de redução dos dois pares redox envolvidos na reação.
U4+ + 2 Ce4+ + 2 H2O ⇌ UO2 2+ + 2 Ce3+ + 4 H+
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
No que concerne a volumetria, gravimetria e potenciometria, julgue o item a seguir.
Situação hipotética: Um minério contendo magnetita (Fe3O4) foi analisado pela dissolução de uma amostra em HCl concentrado, o que resultou em uma mistura de Fe2+ e Fe3+. Depois de adicionado HNO3 para oxidar o Fe2+ a Fe3+, a solução resultante foi diluída com água e todo o Fe3+ foi precipitado como Fe(OH)3 pela adição de NH4OH. Após filtragem e enxágue, o resíduo foi calcinado, resultando em Fe2O3 puro. Assertiva: Nesse caso, a massa de Fe3O4 presente na amostra é corretamente calculada multiplicando-se por 2/3 a massa de Fe2O3 obtida ao final do processo.
Situação hipotética: Um minério contendo magnetita (Fe3O4) foi analisado pela dissolução de uma amostra em HCl concentrado, o que resultou em uma mistura de Fe2+ e Fe3+. Depois de adicionado HNO3 para oxidar o Fe2+ a Fe3+, a solução resultante foi diluída com água e todo o Fe3+ foi precipitado como Fe(OH)3 pela adição de NH4OH. Após filtragem e enxágue, o resíduo foi calcinado, resultando em Fe2O3 puro. Assertiva: Nesse caso, a massa de Fe3O4 presente na amostra é corretamente calculada multiplicando-se por 2/3 a massa de Fe2O3 obtida ao final do processo.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container