Foram encontradas 40 questões.
Considere o rótulo do reagente abaixo para calcular qual será o volume de ácido clorídrico concentrado que deverá ser usado para preparar 250,0mL de solução de ácido clorídrico na concentração de 0,5 mol.L-1.
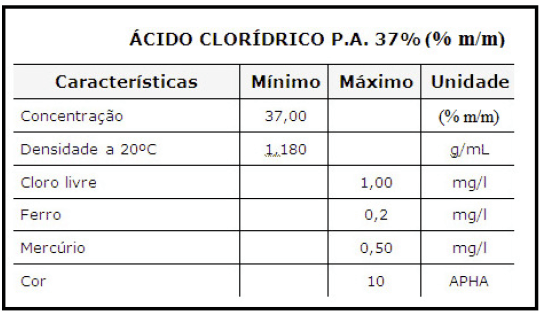
O volume necessário é de:
Provas
Analise o espectro abaixo:
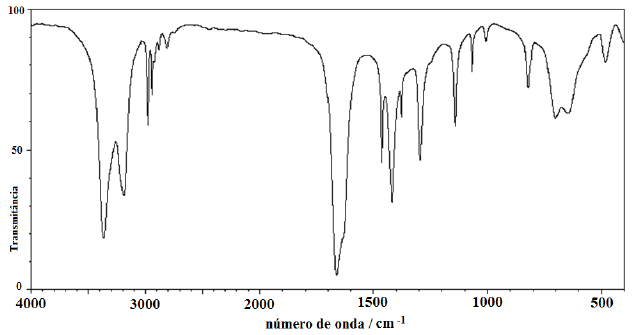
Pode-se afirmar que o espectro acima se refere a uma:
Provas
Em relação à espectroscopia no infravermelho é incorreto afirmar que:
Provas
Um reagente extremamente puro teve seu rótulo rasurado e as informações a respeito do nome, massa molar e fórmula química foram perdidas. A fim de identificar o reagente uma pequena amostra foi submetida a uma análise por infravermelho. O espectro obtido foi:
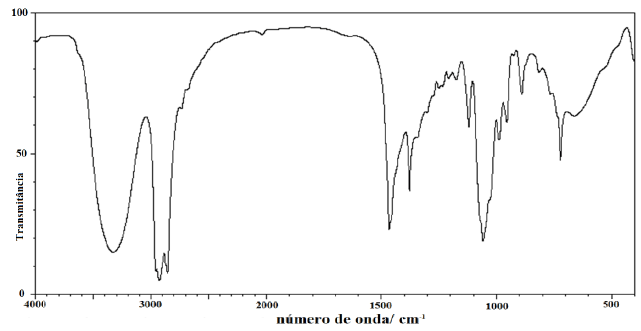
Pode-se afirmar que o reagente referente ao espectro acima é:
Provas
Considere espectro de infravermelho abaixo:
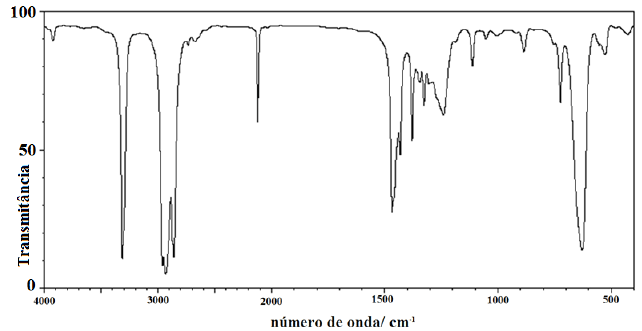
Pode-se afirmar que o composto referente ao espectro acima é:
Provas
A respeito da espectrofotometria UV/VIS é incorreto afirmar que:
Provas
A absortividade molar de certo composto A em 370 nm é igual a 3200 cm-1/(mol/L). A faixa linear adequada para quantificação deste composto é de 0,05 – 0,90 de absorbância. Três amostras líquidas distintas foram submetidas a medidas de absorbância no comprimento de onda supracitado usando uma cubeta de 15 mm de caminho ótico. Os dados obtidos por espectrofotometria estão na tabela abaixo:
| AMOSTRA | ABSORBÂNCIA |
| 1 | 0,33 |
| 2 | 0,48 |
| 3 | 0,70 |
Considerando que a absorbância exibida na tabela é oriunda apenas do composto A, a concentração (mmol/L) deste composto nas amostras 1, 2 e 3 são, respectivamente:
Provas
Considere uma solução A que apresenta 82% de transmitância numa cubeta de 1,5cm de caminho ótico. A alternativa que representa o comprimento da cubeta (caminho ótico) para que se tenha 82% de transmitância triplicando-se a concentração da Solução A é (A solução segue a lei de Lambert-Beer):
Provas
Uma análise espectrofotométrica foi realizada numa certa amostra para determinação do teor de cobre. Os seguintes procedimentos foram adotados:
1- Pesou-se 9,000 g de amostra e a mesma foi tratada com ácido sulfúrico em recipiente adequado (convertendo todo o cobre em CuSO4).
2- Todo o conteúdo do procedimento 1 foi transferido para um balão volumétrico 200mL e completado com água.
3- Uma alíquota da solução obtida em 2 foi usada para leitura direta no espectrofotômetro.
4- Uma curva analítica foi construída com um reagente de CuSO4 para determinação do teor de cobre na amostra.
As absorbâncias dos pontos da curva e da amostra foram obtidas no comprimento de onda igual a 670 nm. Os dados obtidos foram:
| [CuSO4]/ mol.L-1 | ABSORVÂNCIA |
| 0,00 | 0,000 |
| 0,10 | 0,355 |
| 0,20 | 0,723 |
| 0,30 | 1,025 |
| 0,40 | 1,435 |
| 0,50 | 1,756 |
| 0,000 | 0,850 |
Admitindo-se que a única espécie absorvente em 670 nm pós-tratamento advém apenas do sulfato de cobre formado e o “branco” tem valor igual à zero, o teor de cobre (%m/m) na amostra é de:
Provas
Duas amostras aquosas distintas, sulfato ferroso e peróxido de hidrogênio, foram encaminhados para análise em laboratório. Os seguintes procedimentos foram realizados determinação da concentração de seus respectivos analitos de interesse:
1) A amostra 1 é uma solução contendo apenas sulfato ferroso diluído em água. Para a realização da titulação foram tomados 10,00mL da amostra 1. A titulação ocorreu em meio ácido e foram consumidos 37,20mL de permanganato de potássio padronizado de concentração igual a 0,02 mol.L-1 para atingir o ponto final da titulação.
2) A amostra 2 é uma solução contendo apenas peróxido de hidrogênio diluído em água. Para a realização da titulação foram tomados 10,00mL da amostra 1. A titulação ocorreu em meio ácido e foram consumidos 25,30mL de permanganato de potássio padronizado de concentração igual a 0,02 mol.L-1 para atingir o ponto final da titulação.
Após realizar os devidos cálculos pode-se afirmar que a concentração, em g/L, de sulfato ferroso (amostra 1) e peróxido de hidrogênio (amostra 2) são, respectivamente:
Provas
Caderno Container