Foram encontradas 150 questões.
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(C) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
Sabendo-se que o número de átomos de oxigênio ligados ao nitrogênio no ácido HNO3 é maior que no ácido HNO2, é possível concluir que o HNO3 é um ácido mais forte que o HNO2.
Provas
Um químico recebeu uma amostra sólida contendo uma mistura de substâncias orgânicas. Após separação dos componentes da mistura (total de três) e purificação das substâncias, foram realizados testes em laboratório e obtidos diferentes espectros dos compostos. Os resultados foram registrados, alguns dos quais são descritos a seguir.
Substância 1: é insolúvel em água, solúvel em solução aquosa de NaOH a 5%, mas insolúvel em solução aquosa de NaHCO3 a 5%.
Substância 2: o espectro de infravermelho apresenta banda larga em torno de 3.000 cm-1.
Substância 3: o espectro de hidrogênio de ressonância magnética nuclear apresenta dois sinais: um quarteto e um tripleto.
Acerca das substâncias acima descritas e de possíveis testes a serem realizados, julgue o seguinte item.
A substância 1 corresponde a um ácido forte.
Provas
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(C) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
Considerando a equação química geral da obtenção de energia a partir da queima de combustíveis fósseis, conclui-se que, na queima de qualquer combustível fóssil, !$ \alpha + \beta = \gamma + \eta !$.
Provas
Provas

Provas
Provas
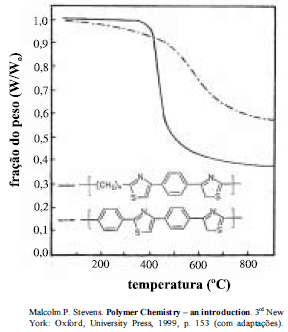
Com relação ao gráfico acima, que representa o comportamento de dois polímeros distintos em uma análise termogravimétrica (TGA), julgue o item seguinte.
É possível diferenciar os dois polímeros utilizando-se ressonância magnética nuclear.
Provas

David Harvey. Modern analytical chemistry. 1st ed. McGraw-
Hill Higher Education, 2000, p. 573 (com adaptações).
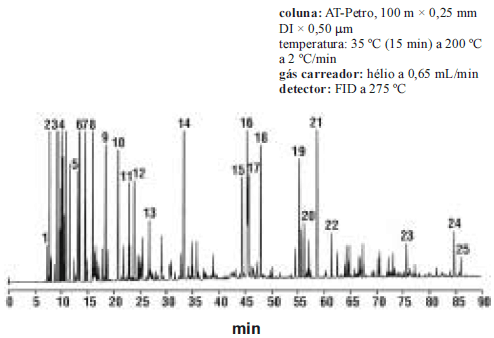
A figura acima mostra um cromatograma obtido em uma análise de gasolina isenta de chumbo por cromatografia gasosa, bem como algumas características dessa corrida cromatográfica. Tendo essa figura como referência, julgue o seguinte item.
A coluna utilizada possui 100 m de comprimento, 250 m de diâmetro interno e 500 nm de diâmetro de partícula.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
A constante de equilíbrio da reação que corresponde à titulação do 2.º hidrogênio do ácido sulfúrico, ou seja, !$ HSO^-_4+OH^- \rightleftharpoons SO^{2-}_4+H_2O !$, é igual a !$ 1 \times 10^{12} !$.
Provas
Provas
Caderno Container