Foram encontradas 700 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
A pressão de vapor de uma substância em sistemas líquido-vapor,
após estabelecido o equilíbrio, corresponde à tendência que suas
moléculas possuem de passar para a fase de vapor a uma
determinada temperatura. A pressão de vapor sobre a solução é
mais baixa do que a pressão de vapor do solvente puro.
O quadro a seguir apresenta as concentrações de cinco soluções ideais obtidas com diferentes solutos totalmente dissociados.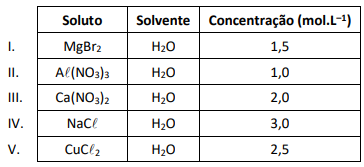
A solução que apresenta a menor pressão de vapor é a
O quadro a seguir apresenta as concentrações de cinco soluções ideais obtidas com diferentes solutos totalmente dissociados.

A solução que apresenta a menor pressão de vapor é a
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaEletroquímica
A pilha comum, também denominada pilha de Leclanché, é
constituída por um cilindro de zinco separado do eletrodo central
que consiste em grafite recoberto por dióxido de manganês,
carvão em pó e uma pasta com cloreto de zinco e cloreto de
amônio.
A equação global de funcionamento da pilha de Leclanché está
representada a seguir.
Zn (s) + 2MnO2 (aq) + 2NH4+ (aq) → Zn2+ (aq) + Mn2O3 (s) + 2NH3 (g) + H2O (ℓ) Essa pilha não é recarregável e deixa de funcionar quando todo o dióxido de manganês é consumido. Sobre o funcionamento da pilha de Leclanché, analise as afirmativas a seguir.
I. No anodo ocorre a oxidação do zinco, liberando dois elétrons. II. No cátodo ocorre a redução do manganês, liberando dois elétrons. III. No polo negativo, o íon amônio sofre oxidação.
Está correto o que se afirma em
Zn (s) + 2MnO2 (aq) + 2NH4+ (aq) → Zn2+ (aq) + Mn2O3 (s) + 2NH3 (g) + H2O (ℓ) Essa pilha não é recarregável e deixa de funcionar quando todo o dióxido de manganês é consumido. Sobre o funcionamento da pilha de Leclanché, analise as afirmativas a seguir.
I. No anodo ocorre a oxidação do zinco, liberando dois elétrons. II. No cátodo ocorre a redução do manganês, liberando dois elétrons. III. No polo negativo, o íon amônio sofre oxidação.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Biomaterial é qualquer material que tenha aplicação biomédica.
Em implantes vasculares como a reposição de artérias de menores
diâmetros, é usado o politetrafluoroetileno.
Assinale a opção que indica a reação de obtenção desse polímero, a partir de seu monômero.
Assinale a opção que indica a reação de obtenção desse polímero, a partir de seu monômero.
Provas
Questão presente nas seguintes provas
A Organização Mundial de Saúde (OMS) indica o consumo de até
2 gramas de íon sódio proveniente de sal comum por dia, por
pessoa.
Considerando o sal comum formado apenas por cloreto de sódio, a quantidade máxima de sal que pode ser utilizada por dia, por pessoa, segundo a OMS é de, aproximadamente,
Dados: massas molares (g.mol-1): Na =23; Cℓ =35,5.
Considerando o sal comum formado apenas por cloreto de sódio, a quantidade máxima de sal que pode ser utilizada por dia, por pessoa, segundo a OMS é de, aproximadamente,
Dados: massas molares (g.mol-1): Na =23; Cℓ =35,5.
Provas
Questão presente nas seguintes provas
Os compostos anfetamínicos atuam como estimulantes do sistema
nervoso central, sendo uma das suas principais características a
eliminação da sonolência. A anfetamina é rapidamente absorvida
após a administração oral, distribuindo-se, preferencialmente, no
cérebro, rins e pulmões. Os compostos resultantes da sua
biotransformação, bem como a substância alterada são
excretados pela urina. Sabe-se ainda que a anorexia causada por
esses compostos pode provocar uma cetose, com consequente
acidificação da urina.
FARIAS,R.F. Introdução à Química Forense. 3ª edição. Campinas, SP: Editora Átomo, 2010. p. 38-39 (adaptado).
Considere o pH 6,0 da urina um valor dentro dos padrões. A urina de um indivíduo que sofre de anorexia, após consumo de anfetamina, pode ter
FARIAS,R.F. Introdução à Química Forense. 3ª edição. Campinas, SP: Editora Átomo, 2010. p. 38-39 (adaptado).
Considere o pH 6,0 da urina um valor dentro dos padrões. A urina de um indivíduo que sofre de anorexia, após consumo de anfetamina, pode ter
Provas
Questão presente nas seguintes provas
Em um recipiente fechado à determinada temperatura, o equilíbrio 2SO3(g) ⇆ 2SO2(g) + O2(g) é estabelecido com as pressões parciais de SO2 (g) e O2 (g) iguais, respectivamente a 0,8 atm e a 0,4 atm. A pressão total do sistema é de 1,4 atm.
Assinale a opção que indica o valor da constante de equilíbrio em função das pressões.
Assinale a opção que indica o valor da constante de equilíbrio em função das pressões.
Provas
Questão presente nas seguintes provas

O gás CO2 de um extintor de incêndio é mais denso do que o ar. À medida que o CO2 sai do extintor, resfria-se significativamente. O vapor d´água no ar é condensado pelo CO2 frio e forma uma nuvem branca.
O fator que faz com que o gás que sai do extintor seja mais denso que o ar é a
Provas
Questão presente nas seguintes provas
Os elementos do grupo 17 (7A) da Classificação Periódica dos
Elementos são conhecidos como halogênios, termo que significa
formadores de sal.
Dentre os halogênios, considere o flúor, o cloro, o bromo e o iodo. Sobre esses elementos, analise as afirmativas a seguir.
I. Quanto maior o raio atômico do halogênio, menor a sua energia de ionização. II. O halogênio de maior densidade, entre os citados, é o iodo. III. O cloro é um gás a 25°C e 1 atm.
Está correto o que se afirma em
Dentre os halogênios, considere o flúor, o cloro, o bromo e o iodo. Sobre esses elementos, analise as afirmativas a seguir.
I. Quanto maior o raio atômico do halogênio, menor a sua energia de ionização. II. O halogênio de maior densidade, entre os citados, é o iodo. III. O cloro é um gás a 25°C e 1 atm.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A geometria molecular interfere diretamente na polaridade e na
solubilidade em água de uma substância.
Assinale a opção que indica apenas moléculas lineares.
Assinale a opção que indica apenas moléculas lineares.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O Oceano Atlântico tem, em média, 28 gramas de cloreto de sódio
por 1 quilograma de água.
Assinale a opção que indica a concentração de cloreto de sódio nessa água, em ppm.
Assinale a opção que indica a concentração de cloreto de sódio nessa água, em ppm.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container