Foram encontradas 3.880 questões.
Internet: <brasilescola.uol.com.br>.
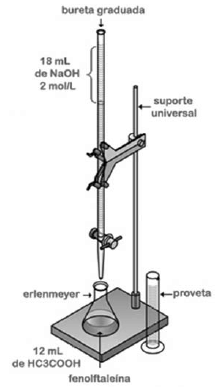
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
Se, na titulação, o ponto de virada ocorreu quando foram consumidos 18 mL de NaOH, então a concentração da solução de CH3COOH é igual a 1 mol/L.
Provas

Internet: <brasilescola.uol.com.br>.
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
A fenolftaleína é um indicador de pH empregado na determinação do ponto de equivalência durante a titulação.
Provas

Internet: <brasilescola.uol.com.br>.
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
A reação de neutralização que ocorre na titulação em questão é corretamente representada pela equação química a seguir, devidamente balanceada.
CH3COOH(aq) + NaOH(aq) → NaC2H3O2(aq) + 2 H2O(ℓ)
Provas

Internet: <brasilescola.uol.com.br>.
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
A solução de NaOH na concentração de 2 mol/L é chamada de titulante.
Provas

Internet: <brasilescola.uol.com.br>.
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
Entre as vidrarias empregadas em análises analíticas, a bureta e a proveta são as que exibem o mais elevado grau de precisão e exatidão, em comparação com o balão volumétrico.
Provas
Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Compostos orgânicos não halogenados com menos de 5 carbonos devem ser descartados na rede de esgoto.
Provas
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
Para a melhor conservação de eletrodos de vidro para a medida de pH, é indicado o uso de soluções de ácido fluorídrico 3 mol/L como líquido de repouso para os eletrodos.
Provas
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Uma solução 0,1 mol/L de NaOH tem concentração em massa maior que 5,0 g/L de NaOH, considerando-se a massa molar do NaOH igual a 40 g/mol.
Provas
O hidróxido de sódio, sólido bastante higroscópico e reativo com o CO2 do ar, é comumente utilizado na padronização e na dosagem de soluções ácidas em laboratórios. Normalmente, para essas titulações, são utilizadas soluções diluídas de NaOH. Em relação a esse assunto, julgue o item a seguir.
Quanto maior a massa molar de um reagente, maior será o erro relativo associado com a pesagem desse reagente, principalmente no preparo de soluções mais diluídas.
Provas
Tendo em vista que o sistema esquelético é responsável por sustentar e dar forma ao corpo, além de proteger os órgãos internos, julgue o próximo item.
O esqueleto humano adulto é dividido em esqueletos axial e apendicular. O esqueleto axial é composto por estruturas ósseas situadas no eixo central do corpo ou próximas a esse eixo.
Provas
Caderno Container