Foram encontradas 352 questões.
Nos polímeros condutores, a flexibilidade e a facilidade de processamento típicas dos polímeros são combinadas com propriedades ópticas e eletrônicas de metais e semicondutores. Nesse tipo de polímero, a presença de ligações duplas alternadas faz que os elétrons !$ \pi !$ estejam deslocalizados devido à ressonância, efeito responsável pela condutividade elétrica do material. O poliacetileno, polímero de adição do acetileno (etino), foi o primeiro polímero condutor sintetizado.
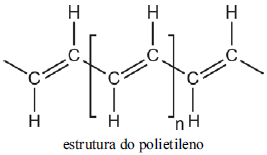
Considerando o texto e a estrutura do polietileno apresentados acima, julgue o item a seguir.
Se for feita polimerização por adição do 1,3-butadieno, será obtido um polímero condutor.
Provas
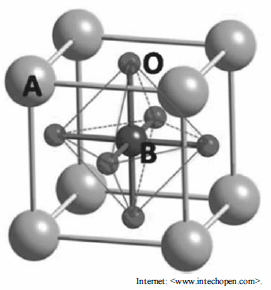
Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
A razão entre o volume do cubo e o volume do octaedro é igual a
Provas

Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
Suponha que uma amostra de água esteja contaminada pela dissolução de uma pequena quantidade de CaTiO3. Nesse caso, o composto que possibilitaria a neutralização dessa amostra de água contaminada é
Provas

Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
Considerando essas informações e que o número de Avogadro seja igual a 6,0 × 1023, julgue o item a seguir.
No CaTiO3, o número de oxidação do Ti é +2.
Provas

Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
Considerando essas informações e que o número de Avogadro seja igual a 6,0 × 1023, julgue o item a seguir.
Se a for a medida da aresta do cubo, então a medida da aresta do octaedro será !$ {\large{\sqrt2 \over 2}}a !$.
Provas

Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
Considerando essas informações e que o número de Avogadro seja igual a 6,0 × 1023, julgue o item a seguir.
Se um plano contém alguma face do octaedro, então esse plano contém um único vértice do cubo.
Provas

Em 2013, uma das descobertas de maior importância do ponto de vista tecnológico foi a criação de unidades fotovoltaicas à base de perovskita, termo que designa um tipo de óxido com fórmula geral ABO3, em que A e B representam cátions metálicos. Um exemplo típico é o CaTiO3. A unidade básica do cristal de uma perovskita consiste na estrutura cúbica mostrada na figura acima, em que cada um de oito cátions “A” ocupa um dos vértices do cubo; seis íons oxigênio estão nos centros das faces do cubo, formando um octaedro regular; e um cátion “B” está no centro do cubo.
Considerando essas informações e que o número de Avogadro seja igual a 6,0 × 1023, julgue o item a seguir.
O número de átomos de cálcio presentes em 27,2 g de CaTiO3 é 1,2 × 1023.
Provas

A figura acima ilustra a alquilação de Friedel-Crafts, uma reação de substituição eletrolítica que ocorre entre um anel aromático e um cloreto de alquila. O AlCl3 é o catalisador mais usualmente empregado nesse tipo de reação. Conforme mostrado na reação a seguir, o AlCl3 liga-se ao cloro do cloreto de alquila e libera um carbocátion, que será o responsável pelo ataque eletrofílico ao anel aromático.
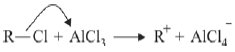
entalpias padrão de formação a 25 ºC (ΔH0f)
| composto | fórmula molecular |
ΔH0f (kJ/mol) |
|
benzeno |
C6H6(l) |
49 |
|
cloreto de metila |
CH3Cl(g) |
-82 |
|
tolueno (metilbenzeno) |
C6H5CH3(l) |
12 |
|
ácido clorídrico |
HCl(g) |
-92 |
Considerando, além das informações do texto e da tabela acima, que as alquilações de Friedel-Crafts sejam de ordem um com relação ao composto aromático e de ordem um com relação ao cloreto de alquila, e que o grupo –OH seja um orientador orto/para dirigente, julgue o item a seguir.
O AlCl3 atua como um ácido de Lewis em reações de alquilação de Friedel-Crafts.
Provas

A figura acima ilustra a alquilação de Friedel-Crafts, uma reação de substituição eletrolítica que ocorre entre um anel aromático e um cloreto de alquila. O AlCl3 é o catalisador mais usualmente empregado nesse tipo de reação. Conforme mostrado na reação a seguir, o AlCl3 liga-se ao cloro do cloreto de alquila e libera um carbocátion, que será o responsável pelo ataque eletrofílico ao anel aromático.
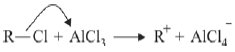
entalpias padrão de formação a 25 ºC (ΔH0f)
| composto | fórmula molecular |
ΔH0f (kJ/mol) |
|
benzeno |
C6H6(l) |
49 |
|
cloreto de metila |
CH3Cl(g) |
-82 |
|
tolueno (metilbenzeno) |
C6H5CH3(l) |
12 |
|
ácido clorídrico |
HCl(g) |
-92 |
Considerando, além das informações do texto e da tabela acima, que as alquilações de Friedel-Crafts sejam de ordem um com relação ao composto aromático e de ordem um com relação ao cloreto de alquila, e que o grupo –OH seja um orientador orto/para dirigente, julgue o item a seguir.
Na presença do AlCl3, a reação se processa por um caminho que envolve menor energia de ativação quando comparada à reação não catalisada.
Provas

A figura acima ilustra a alquilação de Friedel-Crafts, uma reação de substituição eletrolítica que ocorre entre um anel aromático e um cloreto de alquila. O AlCl3 é o catalisador mais usualmente empregado nesse tipo de reação. Conforme mostrado na reação a seguir, o AlCl3 liga-se ao cloro do cloreto de alquila e libera um carbocátion, que será o responsável pelo ataque eletrofílico ao anel aromático.
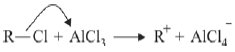
entalpias padrão de formação a 25 ºC (ΔH0f)
| composto | fórmula molecular |
ΔH0f (kJ/mol) |
|
benzeno |
C6H6(l) |
49 |
|
cloreto de metila |
CH3Cl(g) |
-82 |
|
tolueno (metilbenzeno) |
C6H5CH3(l) |
12 |
|
ácido clorídrico |
HCl(g) |
-92 |
Considerando, além das informações do texto e da tabela acima, que as alquilações de Friedel-Crafts sejam de ordem um com relação ao composto aromático e de ordem um com relação ao cloreto de alquila, e que o grupo –OH seja um orientador orto/para dirigente, julgue o item a seguir.
Os valores de entalpias de formação dos compostos envolvidos na reação apresentada abaixo permitem concluir que a reação é endotérmica.
C6H6(l) + CH3Cl(g) !$ \rightarrow !$ C6H5CH3(l) + HCl(g)
Provas
Caderno Container