Foram encontradas 13.435 questões.
Provas
Provas
Provas
Em um processo reversível, a variação no sistema é feita de tal maneira que ele possa ser restaurado ao seu estado original exatamente pela reversão da variação. Um exemplo de processo reversível que ocorre a temperatura constante, no qual as fases estão em equilíbrio, é a água entrando em ebulição a 100º C. Qual a variação de entropia quando 1 mol de água for convertido em 1 mol de vapor a 1 atm de pressão?
Dado: ΔHvaporização (H2O) = +40,67 kJ mol-1
Provas
Para a equação química abaixo, ocorrendo a pressão constante e temperatura de 25 ºC, o valor de ∆G, em KJ, é aproximadamente
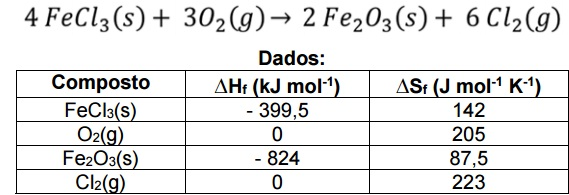
Provas
Acerca da termoquímica, da espontaneidade de reações e da ação de catalisadores, julgue o item a seguir.
Um processo é espontâneo se é acompanhado por uma diminuição na entropia total do sistema e das vizinhanças. Dessa forma, os processos espontâneos à temperatura e pressão constantes são acompanhados por um aumento da energia livre, ou seja, a direção da mudança espontânea é a direção do aumento da energia livre.
Provas
As atividades realizadas nos laboratórios didáticos de Química precisam ser acompanhadas do descarte correto dos resíduos produzidos durante as aulas experimentais, sendo importante classificar os resíduos e escolher o tratamento mais adequado. Nesse sentido, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
1. Resíduos básicos concentrados, p. ex. aminas.
2. Resíduos fortemente oxidantes em solução, p. ex. permanganato.
3. Resíduo de mercúrio metálico.
4. Resíduo contendo sais de cianeto em solução aquosa diluída.
( ) Tratar com sulfito de sódio e depois ajustar o pH entre 7 e 9.
( ) Recobrir o resíduo com enxofre em pó e armazenar.
( ) Diluir até obtenção de uma solução com pelo menos 50% de água (em volume) e, em seguida, ajustar o pH entre 7 e 9.
( ) Adicionar 1 grama de NaOH por 100 mL de solução. Adicionar água sanitária.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
Provas
O ácido nítrico “branco” (100% puro; P.E. = 83 ºC) pode ser obtido em laboratório por destilação de uma mistura de \( KNO_3 \) e \( H_2SO_4 \), como mostra a reação a seguir:
\( KNO_3 + H_2SO_4 → HNO_3 + KHSO_4 \)
Tendo em vista que o \( HNO_3 \) é decomposto por aquecimento a \( NO_2 \) e \( H_2O \), assinale a alternativa que apresenta a técnica de destilação que deve ser utilizada nesse processo.
Provas
O ácido fosfórico (\( H_3PO_4 \)) de alta pureza é obtido por via seca ou térmica, pela combustão do fósforo elementar e posterior hidratação do \( P_2O_5 \), de acordo com as reações abaixo:
\( 4P + 5O_2 → 2P_2O_5 \;\; ΔH= -720 kcal \)
\( P_2O_5 + 3H_2O → 2H_3PO_4 \;\; ΔH= -45 kcal \)
Nesse processo, de acordo com as equações acima, assinale a alternativa que apresenta a quantidade de calor liberado na formação do \( H_3PO_4 \) (em kcal/mol).
Provas
Foi requisitado a um técnico de laboratório que preparasse uma solução de hidróxido de amônio, a partir de uma solução comercial concentrada, cujo rótulo contém as informações ao lado:
Dados: MM(\( NH_3 \)) = 17g/mol
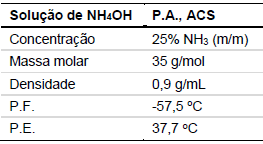
Assinale a alternativa que indica o volume aproximado da solução comercial (em mL) que o técnico deve utilizar para obter 5 litros de uma solução de \( NH_4OH \) 1 mol/L.
Provas
Caderno Container