Foram encontradas 40 questões.
Segundo a RDC 658/2022 o gerenciamento de riscos da qualidade é um processo sistemático de avaliação, controle, comunicação e revisão de riscos para a qualidade do medicamento. Considerando que as boas práticas de fabricação se aplicam a todo o ciclo de vida de um medicamento, incluindo seu desenvolvimento, observe as alternativas abaixo e avalie se são verdadeiras (V) ou falsas (F):
I- A avaliação de riscos na etapa de desenvolvimento tecnológico pode auxiliar na avaliação dos atributos dos materiais e dos parâmetros de processo e a forma como estes fatores impactam na qualidade, segurança e eficácia do medicamento em desenvolvimento.
II- A definição de um design space por meio de análise de riscos se tornou mandatória após a implementação da RDC 658/2022. A partir da vigência desta resolução, devem ser apresentadas análises multivariadas que assegurem que as faixas de trabalho são adequadas para atingir a especificação do medicamento.
III- As saídas e resultados do gerenciamento de riscos devem ser revisadas para considerar o conhecimento adquirido no ciclo de vida do medicamento e a experiência em seu processo produtivo. Em um processo de maior maturidade a reconsideração de riscos pode ocorrer para suportar a tomada de decisões.
A ordem correta, de cima para baixo, é:
Provas
Provas
Provas
I- A fotodegradação pode ocorrer por diversos mecanismos, alguns dos quais não são dependentes da quantidade de luz que o sistema é exposto. Assim, pode-se inferir que algumas reações de fotodegradação ocorrem mesmo se a exposição for a pequena quantidade de luz.
II- A luz pode atuar apenas como promotor de uma reação de degradação do ativo em um medicamento, que continua a ocorrer mesmo depois de cessada a exposição.
III- O estudo de fotoestabilidade, de acordo com o preconizado pela RDC 318 de 06 de novembro de 2019, baseia-se na exposição do produto a uma grande quantidade de luz em um curto período de tempo ao passo que na vida real do medicamento a exposição se dá a uma pequena quantidade de luz por um longo período de tempo.
IV- Em um estudo de fotoestabilidade o medicamento em desenvolvimento deve ser exposto tanto à incidência de luz visível (cuja unidade de luminosidade é o lux) quanto para a luz ultravioleta (cuja unidade de radiação é watt.horas/m2).
A ordem correta, de cima para baixo, é:
Provas
Provas
Provas
Provas
Provas
I) visa a inovação, a melhoria contínua e o fortalecimento do vínculo entre o desenvolvimento farmacêutico e as atividades produtivas industriais.
II) não integra os requisitos necessários para o planejamento e para a execução de um projeto de desenvolvimento farmacêutico.
III) rege somente os projetos que gerem medicamentos experimentais.
IV) deve gerenciar todas as informações que influenciem na qualidade, eficácia e segurança do medicamento em desenvolvimento.
V) garante que o conhecimento de produtos e processos seja gerenciado em todas as etapas do ciclo de vida do medicamento.
Sobre as afirmativas acima, é correto afirmar que apenas:
Provas
Avalie os resultados abaixo, conforme o preconizado pela RDC 318 de 6 de novembro de 2019, que estabelece os critérios para a realização de estudos de estabilidade de insumos farmacêuticos ativos e medicamentos, exceto biológicos, e dá outras providências.
Resultados de estudo de estabilidade acelerada (40°C ± 2°C / 75% UR ± 5% UR) do medicamento X 150 mg/comprimidos
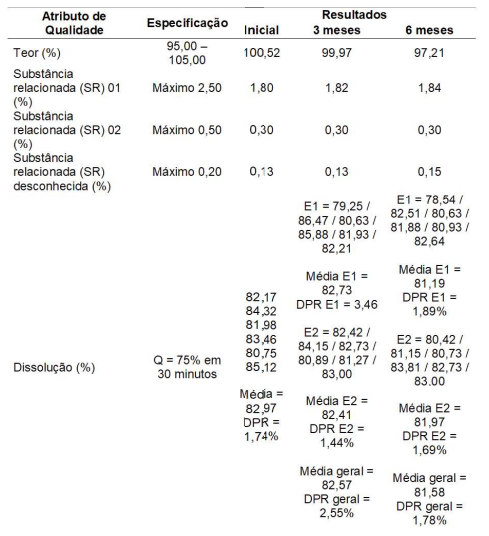
Sobre o estudo de estabilidade acima, avalie se são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I – O medicamento X apresenta queda de teor no estudo de estabilidade acelerada. Por este motivo o estudo de estabilidade está reprovado.
II – É uma hipótese plausível que a SR 02 seja oriunda unicamente da síntese do IFA do medicamento.
III – É uma hipótese plausível que a SR 01 seja oriunda da degradação do fotolítica do IFA.
IV – Pelo conjunto dos resultados, pode-se concluir que o estudo de estabilidade acelerada atende aos requisitos para sua aprovação em conformidade com a zona climática II.
V – O estudo está aprovado frente aos requisitos da RDC 318/2019.
VI – Os resultados do ensaio de dissolução nas frequências de 3 e 6 meses estão reprovados em primeiro estágio.
De cima para baixo a ordem correta é:
Provas
Caderno Container