Foram encontradas 57 questões.
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
A RDC N°17, de 16 de abril de 2010, preceitua que a
qualificação e a validação não devem ser consideradas
exercícios únicos. Após a aprovação do relatório de
qualificação e/ou validação deve haver um programa
contínuo de monitoramento, o qual deve ser embasado em
uma revisão periódica. O compromisso da manutenção da
situação de qualificação/validação deve estar descrito nos
documentos relevantes da empresa, como:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
De acordo a Resolução - RDC N° 17, de 16 de abril de 2010
pode-se definir validação como o ato documentado que
atesta que qualquer procedimento, processo, equipamento,
material, atividade ou sistema realmente e consistentemente
leva aos resultados esperados. Ainda, em consonância com
essa mesma norma, existem diferentes tipos e abordagens
com relação à validação. Relacione a coluna da esquerda
(tipos e abordagem) com a coluna da direita (definição) e
estabeleça a correta correspondência
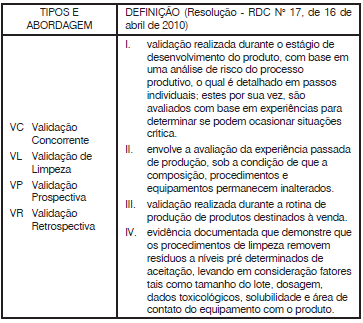
Estão corretas as associações

Estão corretas as associações
Provas
Questão presente nas seguintes provas
- Análises Clínicas
- Controle de QualidadeControle de Qualidade Industrial
- Controle de QualidadeControle de Qualidade Laboratorial
As operações de produção devem seguir Procedimentos
Operacionais Padrão (POPs) escritos, claramente definidos,
aprovados e em conformidade com o registro aprovado, com
o objetivo de obter produtos que estejam dentro dos padrões
de qualidade exigidos. Para evitar a ocorrência de
contaminação cruzada, técnicas apropriadas ou medidas
organizacionais devem ser adotadas, como as afirmativas a
seguir apresentam, à exceção de uma. Assinale-a.
Provas
Questão presente nas seguintes provas
A esterilização é um processo de destruição de todas as
formas de vida microbiana: bactérias, fungos, vírus e esporos
mediante a aplicação de agentes físicos, químicos ou físico-químicos.
Sobre o tema, selecione a afirmativa incorreta.
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
De acordo com o que estabelece a RDC N°17, de 16 de abril
de 2010, o fabricante é responsável pela qualidade dos
medicamentos por ele fabricados, assegurando que sejam
adequados aos fins a que se destinam, cumpram com os
requisitos estabelecidos em seu registro e não coloquem os
pacientes em risco por apresentarem segurança, qualidade
ou eficácia inadequada. O cumprimento deste objetivo é
responsabilidade:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
Segundo a RDC N°17, de 16 de abril de 2010, a validação de
processos e sistemas é fundamental para se atingir os
objetivos. É por meio do projeto e validação que um
fabricante pode estabelecer com confiança que os produtos
fabricados irão consistentemente atender as suas
especificações.
A documentação associada à validação deve incluir:
I. Procedimentos Operacionais Padrão (POP).
II. especificações.
III. Plano Mestre de Validação (PMV).
IV. protocolos e relatórios de qualificação.
V. protocolos e relatórios de validação.
Assinale:
I. Procedimentos Operacionais Padrão (POP).
II. especificações.
III. Plano Mestre de Validação (PMV).
IV. protocolos e relatórios de qualificação.
V. protocolos e relatórios de validação.
Assinale:
Provas
Questão presente nas seguintes provas
A Garantia da qualidade é um conceito amplo e deve cobrir
todos os aspectos que influenciam individual ou
coletivamente a qualidade de um produto. Assinale a
alternativa incorreta em um sistema de garantia da
qualidade relacionado à fabricação de medicamentos.
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
De acordo com a RDC N°17, de 16 de abril de 2010, são
exemplos de itens que devem ser verificados por ocasião da
aplicação do protocolo de Qualificação de Instalação (QI):
Provas
Questão presente nas seguintes provas
São considerados pré-requisitos fundamentais para dar
iniciar aos procedimentos de validação de processo:
I. Métodos analíticos validados.
II. Equipamentos Qualificados (Instalação, Operação e Desempenho).
III. Procedimentos operacionais descritos e todos os funcionários treinados.
IV. Todos os fornecedores qualificados.
Assinale:
I. Métodos analíticos validados.
II. Equipamentos Qualificados (Instalação, Operação e Desempenho).
III. Procedimentos operacionais descritos e todos os funcionários treinados.
IV. Todos os fornecedores qualificados.
Assinale:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
Em consonância com as BPF (Resolução da ANVISA, RDC
17 DE 2010), a empresa deve identificar quais os trabalhos
de qualificação e validação são necessários para comprovar
que todos os aspectos críticos de operação estejam sob
controle. A qualificação e a validação devem estabelecer e
fornecer evidências documentadas dos seguintes itens,
exceto,:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container