Foram encontradas 57 questões.
- Análises Clínicas
- Bioestatística
- Controle de QualidadeControle de Qualidade Industrial
- Controle de QualidadeControle de Qualidade Laboratorial
No Controle Estatístico de Processo, o gráfico de controle é
utilizado na detecção de alterações inusitadas de uma ou
mais características de um processo ou produto. Em outras
palavras, é uma ferramenta estatística que desperta para a
presença de causas especiais grandes na linha de produção.
A esse respeito, assinale a afirmativa incorreta.
Provas
Questão presente nas seguintes provas
A Metodologia de Aminação Redutiva é utilizada para a produção de algumas vacinas conjugadas.
Com relação a essa metodologia, analise as afirmativas a seguir.
I. Na metodologia de aminação redutiva a proteína carreadora é polissubstituída com cadeias de carboidrato, originando uma estrutura denominada neoglicoproteína.
II. São introduzidos grupamentos funcionais aldeídos terminais nas moléculas de polissacarídeo, por meio de oxidação seletiva com periodato de sódio (NaIO4), antes da conjugação com a proteína carreadora.
III. A reação de conjugação ocorre entre os grupamentos aldeídos gerados nas moléculas de polissacarídeo e os grupamentos aminos presentes na molécula de proteína.
Provas
Questão presente nas seguintes provas
Em consonância com as Boas Praticas de Fabricação (BPF),
a empresa deve identificar quais os trabalhos de qualificação
e validação são necessários para comprovar que todos os
aspectos críticos de operação estejam sob controle. Os
elementos chave de um programa de qualificação e
validação de uma empresa devem ser claramente definidos e
documentados em um:
Provas
Questão presente nas seguintes provas
Durante a concepção dos Protocolos de Validação de
limpeza, é imprescindível a etapa de definição do insumo
farmacêutico ou produto como “pior caso". De acordo com
o que preconiza as normas e legislações, e demais
referências pertinentes, a escolha do pior caso deve ser
baseada:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
A Resolução - RDC N° 17, de 16 de abril de 2010 que
“Dispõe sobre as Boas Práticas de Fabricação de
Medicamentos", determina que qualificação e a validação
devem estabelecer e fornecer evidências documentadas de
que:
I. instalações, utilidades, sistemas computadorizados, equipamentos e processos foram projetados em consonância com as exigências de BPF (qualificação de projeto ou QP).
II. instalações, utilidades, sistemas computadorizados e equipamentos foram construídos e instalados de acordo com as suas especificações de projeto (qualificação de instalação ou QI).
III. instalações, utilidades, sistemas computadorizados e equipamentos operam de acordo com suas especificações planejadas (qualificação de operação ou QO).
IV. uma metodologia analítica e um processo específico produzirá um produto que consistentemente atenda suas especificações e atributos de qualidade (validação de processo ou VP, também chamada em alguns casos de qualificação de desempenho ou QD).
Assinale:
I. instalações, utilidades, sistemas computadorizados, equipamentos e processos foram projetados em consonância com as exigências de BPF (qualificação de projeto ou QP).
II. instalações, utilidades, sistemas computadorizados e equipamentos foram construídos e instalados de acordo com as suas especificações de projeto (qualificação de instalação ou QI).
III. instalações, utilidades, sistemas computadorizados e equipamentos operam de acordo com suas especificações planejadas (qualificação de operação ou QO).
IV. uma metodologia analítica e um processo específico produzirá um produto que consistentemente atenda suas especificações e atributos de qualidade (validação de processo ou VP, também chamada em alguns casos de qualificação de desempenho ou QD).
Assinale:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
A RDC N°17, de 16 de abril de 2010, considera que um
processo específico produzirá consistentemente um produto
que atenda suas especificações e atributos de qualidade.
Nesse artigo referente ao capitulo dedicado a qualificação e
validação, a norma em referência está se referindo a:
Provas
Questão presente nas seguintes provas
Pode-se considerar que um dos desafios da Validação de
Limpeza, é estabelecer procedimentos, capazes de
concentrar de forma satisfatória os resíduos de fármacos
amostrados nos equipamentos, bem como consolidar as
metodologias analíticas capazes de quantificar esses
resíduos que se encontram na maioria das vezes em
baixíssimas concentrações. Na tentativa de reduzir os erros
analíticos, é conveniente que o analista estabeleça técnicas,
com limites de detecção compatíveis com os equipamentos
que estão sendo utilizados nas analises de quantificação
desses resíduos. Limite de Detecção pode ser definido
como:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
De acordo com RDC N°17, de 16 de abril de 2010, as Boas
Praticas de Fabricação de Medicamentos determinam que:
I. todos os processos de fabricação devam ser claramente definidos e sistematicamente revisados em função da experiência adquirida.
II. devem ser capazes de fabricar medicamentos dentro dos padrões de qualidade exigidos, atendendo às respectivas especificações.
III. sejam realizadas as qualificações e validações necessárias.
IV. que seja implantado um sistema capaz de recolher qualquer lote, após sua comercialização ou distribuição, na ocasião da identificação de algum desvio de qualidade. O prazo de recolhimento deverá ser de 45 a 60 dias.
Assinale:
I. todos os processos de fabricação devam ser claramente definidos e sistematicamente revisados em função da experiência adquirida.
II. devem ser capazes de fabricar medicamentos dentro dos padrões de qualidade exigidos, atendendo às respectivas especificações.
III. sejam realizadas as qualificações e validações necessárias.
IV. que seja implantado um sistema capaz de recolher qualquer lote, após sua comercialização ou distribuição, na ocasião da identificação de algum desvio de qualidade. O prazo de recolhimento deverá ser de 45 a 60 dias.
Assinale:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
Com base na Resolução - RDC N° 17, de 16 de abril de 2010
que “Dispõe sobre as Boas Práticas de Fabricação de
Medicamentos", analise a tabela a seguir.
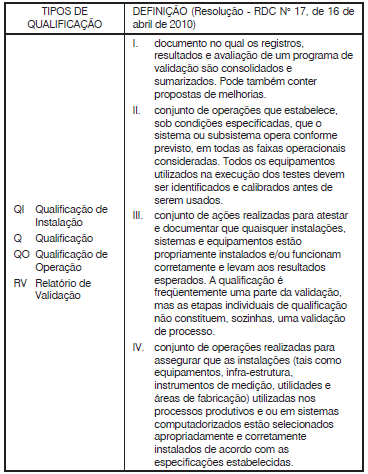
Está correto apenas o que se afirma em

Está correto apenas o que se afirma em
Provas
Questão presente nas seguintes provas
Um aspecto essencial na validação de limpeza é determinar
quanto de limpeza é suficiente. Apesar de oficialmente não
endossar critérios adotados por indústrias farmacêuticas, o
FDA (Food Drug Administration) dos Estados Unidos da
América faz referência a critérios adotados pela empresa Eli
Lilly, que estabelece os seguintes critérios (LeBlanc, 1999):
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
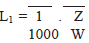
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
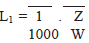
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container