Foram encontradas 20 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma amostra de 10,00 mL contendo Ni2+ foi tratada com 5,00mL de uma solução de EDTA 0,0500 M para complexar todo o Ni2+ e manter um excesso de EDTA em solução.
Esse excesso de EDTA foi então titulado e consumiu 1,00 mL de uma solução de Zn 2+ 0,0500M. A concentração molar de Ni 2+ na amostra original é de:Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Considere a curva de titulação volumétrica pH x V titulante:
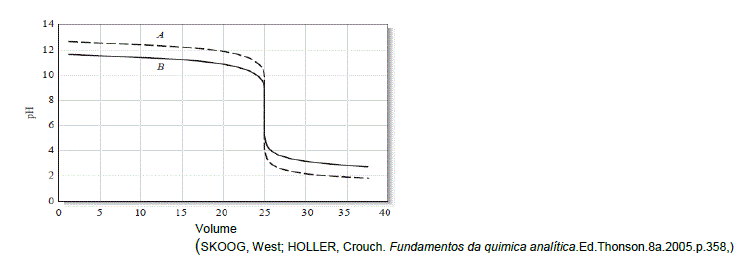
É INCORRETO afirmar que:
Provas
O EDTA é o agente de complexação de uso mais corrente em química analítica. Praticamente todos os elementos da tabela periódica podem ser determinados quantitativamente pelo EDTA através de titulação direta ou por uma sequência de reações indiretas.
O íon metálico listado abaixo que NÃO é complexado pelo EDTA é:
Provas
Um reagente padrão primário é suficientemente puro para ser pesado e usado diretamente. Um padrão primário deverá ser 99,9% puro, ou mais. Não deverá se decompor quando é estocado de modo normal, e deverá ser estável quando é seco por aquecimento ou por vácuo.
Considerando que todos os reagentes abaixo apresentam elevado grau de pureza, qual NÃO é considerado um padrão primário:
Provas
A espectroscopia atômica é uma das ferramentas mais importantes da química analítica devido a sua alta sensibilidade, a sua capacidade de distinguir um elemento de outro em uma amostra complexa, e à possibilidade de se analisarem, simultaneamente, vários elementos.
Com relação aos princípios da técnica de espectroscopia atômica, assinale a alternativa INCORRETA:
Provas
A validação do método é o processo que prova que o método analítico é aceitável para os propósitos a que ele se destina. As exigências de validação de um método para submissão ao órgão adequado incluem estudos de especificidade do método, linearidade, exatidão, precisão, faixa, limite de detecção, limite de quantificação e robustez.
Com relação a esses parâmetros, assinale a alternativa CORRETA:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A tabela a seguir apresenta os valores, em torno do ponto final, de pH por volume de NaOH adicionado, em uma titulação de 1,00 mL de um ácido monoprótico hipotético HA, avolumado com água destilada para 100 mL, com uma solução de NaOH 0,1000 mol/L.
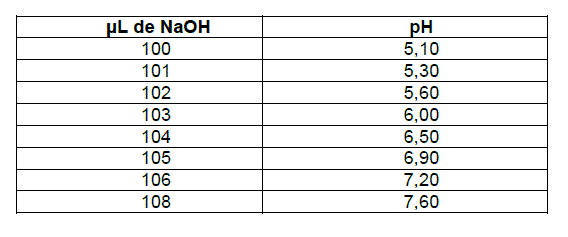
Provas
Ao medir o pH de uma solução de NaOH 50% m/v, utilizando um eletrodo de vidro combinado, um analista encontrou o valor de 7,50. A inconsistência nesse resultado pode ser explicada por:
Provas
Assinale a alternativa em que o procedimento para preparo do branco para determinação do teor de ferro na amostra de minério, baseando-se na reação: Fe 3+ + SCN- --> Fe(SCN)6 3- , está corretamente descrito:
Provas
O teor de ferro em uma amostra de minério de ferro pode ser determinado por Espectrometria de Absorção Molecular (EAM) na região do visível, com base na seguinte reação:
Fe 3+ + SCN- --> Fe(SCN)6 3-Para análise de uma amostra de minério de ferro por EAM, 2 g da mesma foram adequadamente abertos, transferidos para um balão volumétrico de 1 L, que foi completado com água, de maneira a preparar uma solução contendo 2 g de minério/L. Dessa solução, pipetou-se 1 mL para outro balão de 1 L, adicionou-se 20 mL de uma solução de ZnSO4, 10 mL de H2O2 10 Vol., 200 mL de uma solução de KSCN, e completou-se o volume com água, produzindo o que se chamou de solução diluída de amostra. Uma série de padrões foi preparada a partir de uma solução estoque intermediária de 100 μg/mL de Fe 3+ , pipetando-se 1, 2, 3, 4 e 5 mL da mesma para 5 balões volumétricos de 100 mL, adicionando-se a cada balão 2 mL de solução de ZnSO4, 1 mL de H2O2 10 Vol., 20 mL de uma solução de KSCN e completando-se o volume com água, produzindo os padrões 1, 2, 3, 4 e 5, respectivamente. As absorbâncias para os padrões, lidas em um Espectrofotômetro de Absorção Molecular, no comprimento de onda 510 nm, estão apresentadas abaixo:
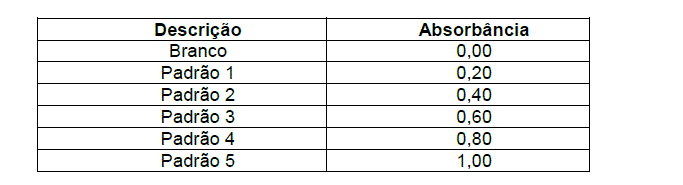
A curva de calibração, construída a partir dos padrões, está representada no gráfico abaixo, bem como sua equação.
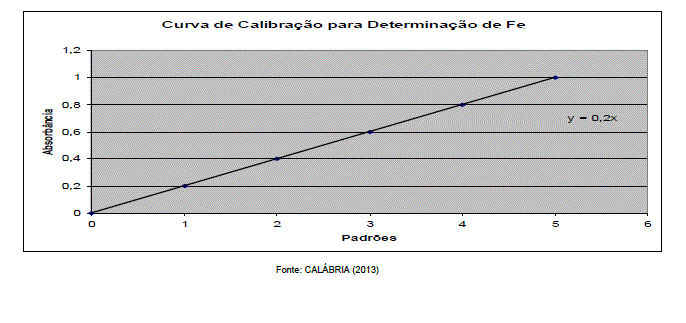
Provas
Caderno Container