Foram encontradas 70 questões.
O potencial de uma célula eletroquímica é a diferença entre o potencial de eletrodo de cada semi-célula. Considere uma célula eletroquímica hipotética constituída por uma semi-célula formada por um eletrodo de cádmio imerso em uma solução com íons Cd2+ na concentração 1,00 mol.L–1 e outra formada por um eletrodo de cobre imerso em uma solução diluída com íons Cu2+ na concentração 0,01 mol.L–1. Os potenciais padrão dos eletrodos nas condições do enunciado são:
Cd2+ + 2e– \(\rightleftharpoons\) Cd E0 = – 0,4030 V
Cu2+ + 2e– \(\rightleftharpoons\) Cu E0 = + 0,3419 V
Nessas condições, o potencial da célula eletroquímica hipotética (em volts), representada por
Cd (s)│Cd2+ (1,00 mol.L–1)││Cu2+ (0,01 mol.L–1)│Cu (s)
é igual a
Provas
Um solução padrão de tiocianato de potássio 0,10 mol.L–1 foi utilizada para determinar a quantidade de íons prata em 100 mL de uma amostra preparada isenta de mercúrio, paládio e sais de metais coloridos. Foram tituladas com agitação alíquotas de 25 mL da amostra utilizando a solução padrão. Cada titulação utilizou 21,5 mL do padrão.
De acordo com os dados, a quantidade (em gramas) de prata presente nos 100 mL é, aproximadamente, de
Massa molar: Ag = 107,87g.mol–1
Provas
O sal de Mohr [Fe(NH4)2(SO4)2] é utilizado para analisar solos com teores de carbono inferiores a 20g/kg. Para ser utilizada como padrão, uma amostra com 15,68 g do sal de Mohr hexaidratado foi calcinada produzindo 2,88 g de óxido de ferro (III).
A pureza da amostra, relacionada ao cátion trivalente do ferro, obtida foi igual a
Massas molares: H = 1 g.mol–1; N = 14 g.mol–1; O = 16 g.mol–1; S = 32 g.mol–1; Fe = 56 g.mol–1
Provas
O metanal (formaldeído) e o etanal (acetaldeído) são compostos tóxicos que causam irritação nos olhos e nas mucosas do trato respiratório. Cada uma dessas substâncias pode sofrer reação de oxidação produzindo compostos que também possuem toxicidade. Outra reação que pode ocorrer envolvendo o formaldeído e o acetaldeído é a condensação aldólica, na qual o aldol formado perde água e forma um composto cujos vapores podem causar severas irritações respiratórias e oculares e, se ingerido, provoca náuseas, vômito e até edema pulmonar.
Os produtos das reações citadas no fragmento acima são, respectivamente,
Provas
O tolueno pode ser classificado como moderadamente tóxico por inalação ou ingestão; a exposição a elevados níveis desse composto pode evoluir para o coma. A oxidação metabólica do tolueno pode produzir compostos excretados pelo organismo, entre eles o representado a seguir.
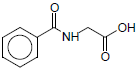
As funções orgânicas presentes no composto são, respectivamente,
Provas
A Resolução n. 357 do Conselho Nacional do Meio Ambiente dispõe sobre a classificação dos corpos de água e sobre as diretrizes ambientais para o seu enquadramento.
Segundo essa resolução, uma amostra de água que apresenta concentração de sais 10g.Kg–1 é classificada como água
Provas
Em uma fazenda foi adicionado, como suplemento à ração do gado, cloreto de amônio. O resíduo desse composto foi lavado com água, resultando em uma solução de cloreto de amônio de concentração 0,016 mol.L–1. Essa solução teve seu pH avaliado para a escolha do método de descarte.
A solução apresentou pH aproximadamente igual a
Constante de hidrólise do sal (nas condições do enunciado) = 5,6 x 10–10 e log 3 = 0,48.
Provas
Minerais contendo cálcio são a principal fonte deste íon em sistemas de água doce. A dureza temporária da água está relacionada com a presença do íon Ca2+ e do íon bicarbonato dissolvidos que podem participar do equilíbrio:
Ca2+ (aq) + 2HCO3 (aq) \(\rightleftharpoons\)CaCO3 (s) + CO2(g) + H2O\(\ell\)
Considerando a formação do carbonato de cálcio neste equilíbrio endotérmica e o Princípio de Le Chatelier, o procedimento utilizado para diminuir a dureza temporária da água é o de
Provas
Materiais dissolvidos no meio aquoso podem provocar a corrosão de antigas tubulações de chumbo em sistemas domésticos de distribuição de água, permitindo que esse elemento, que é tóxico, entre em solução.
Considere as semi-reações de redução a seguir:
| Eº (V) | |
| A\(\ell\)3+ + 3e– \(\rightleftharpoons\) A\(\ell\) | - 1,662 |
| Cd2+ + 2e– \(\rightleftharpoons\) Cd | - 0,4030 |
| Fe3+ + 3e– \(\rightleftharpoons\) Fe | - 0,037 |
| Pb2+ + 2e– \(\rightleftharpoons\) Pb | - 0,1262 |
| Sn2+ + 2e– \(\rightleftharpoons\) Sn | - 0,1375 |
| Zn2+ + 2e– \(\rightleftharpoons\) Zn | - 0,7618 |
A liberação do chumbo para a solução pode ser provocada pela presença do íon:
Provas
Só falta a política de redução de riscos
Entre 1990 e 2010, mais de 96 milhões de pessoas foram afetadas por desastres no Brasil, como demonstra o Atlas dos Desastres Naturais do Brasil. Destas, mais de 6 milhões tiveram de deixar suas moradias, cerca de 480 mil sofreram algum agravo ou doença e quase 3,5 mil morreram imediatamente após os mesmos. Desastres como o de Petrópolis, que resultaram em dezenas de óbitos, não existem em um vácuo. Se por um lado exigem a presença de ameaças naturais, como chuvas fortes, por outro não se realizam sem condições de vulnerabilidade, constituídas através dos processos sociais relacionados à dinâmica do desenvolvimento econômico e da proteção social e ambiental. Isto significa que os debates em torno do desastre devem ir além das cobranças que ano após ano ficam restritas à Defesa Civil.
A redução de riscos de desastres deve hoje constituir o cerne da política brasileira para os desastres. Isto significa combinar um conjunto de políticas não só para o durante os riscos e situações de desastres, o que avançamos bem, mas também e principalmente para o antes e o depois dos mesmos.
Particularmente, após o desastre da Região Serrana (RJ) em 2011, uma série de iniciativas importantes ocorreu. Criou-se o Centro Nacional de Monitoramento e Alerta de Desastres Naturais, a Força-Tarefa de Apoio Técnico e Emergência, a Força Nacional do SUS e reestruturou-se o Centro Nacional de Gerenciamento de Riscos de Desastres. Estas iniciativas ainda estão concentradas no monitoramento, alerta e respostas aos desastres. Faltam políticas integradas para redução de riscos.
Dados do IBGE revelam que apenas 1,2% dos municípios possuíam plano municipal de redução de riscos em 2011. Nos municípios maiores, com mais de 500 mil habitantes, que não ultrapassam quatro dezenas, este percentual superava 50%. De modo inverso, nos municípios menores, com menos de 20 mil habitantes, em torno de quatro mil, este percentual era de 3,3%. É uma situação bastante preocupante relacionada aos municípios de grande porte e drástica nos municípios de pequeno porte.
Há necessidade urgente de se investir em políticas integradas. E que ofereçam suporte aos municípios de menor porte. Na outra ponta, políticas de recuperação e reconstrução após desastres deveriam permitir o retorno à normalidade da vida "cotidiana", não prolongando os efeitos dos desastres, como temos visto.
(Carlos Machado - O Globo, 01/04/2013)
Com relação às formas verbais sublinhadas, é correto afirmar que
Provas
Caderno Container