Foram encontradas 100 questões.
O gás natural possui uma quantidade variável de gás carbônico e gás sulfídrico. O CO2 é indesejável, já que reduz o poder calorífico do gás natural e dificulta o transporte do mesmo sob baixas temperaturas e alta pressão, pois solidifica. Já o gás sulfídrico é extremamente venenoso e corrosivo frente aos equipamentos metálicos. Uma das técnicas utilizadas para retirar esses contaminates gasosos é a absorção física, onde o gás natural passa pelo solvente polietilenoglicol sob altas pressões e baixa temperatura, sendo seletivamente absorvido pelo polímero. O polímero absorvente é sintetizado a partir do óxido de etileno em meio ácido, de acordo com a reação abaixo.
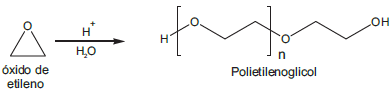
O polietilenoglicol é
Provas
Questão presente nas seguintes provas
Três cubas eletrolíticas ligadas em série, munidas de eletrodos de platina, contêm, respectivamente, soluções aquosas de sulfato cúprico, ácido sulfúrico e nitrato de prata. Após certo tempo de passagem de corrente elétrica, a eletrólise foi interrompida. Sabendo-se que 1,35 g de cobre foi depositado na primeira cuba, analise as afirmativas a seguir.
I – A quantidade de prata depositada na terceira cuba é 4,59 g.
II – Há produção de gás oxigênio apenas na segunda cuba.
III – A quantidade de ácido sulfúrico permanece constante na segunda cuba.
IV – O volume de oxigênio produzido, nas CNTP, na segunda cuba, é de 0,24 L.
Dado: Volume molar dos gases na CNTP = 22,4 L.mol–1
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
O besouro-bombardeiro, cujo nome científico é Brachynus crepitans, possui, no seu abdômen, dois compartimentos distintos que armazenam hidroquinona e peróxido de hidrogênio. Quando ele se sente ameaçado, essas substâncias se misturam e, através de uma catálise enzimática, há a formação de p-benzoquinona, que é expelida sob a forma de uma solução quente, de acordo com a reação abaixo.
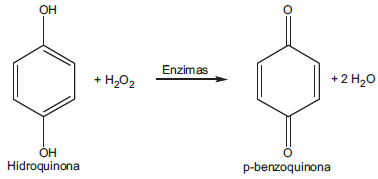
Nessa reação de oxirredução,
Provas
Questão presente nas seguintes provas
Considere que uma solução aquosa de ácido clorídrico reagiu com os seguintes reagentes:
• solução de tiossulfato de sódio;
• dióxido de manganês;
• carbonato de cálcio;
• zinco metálico.
Sobre essas reações, analise as afirmativas a seguir.
I – O ácido clorídrico atua como agente oxidante do tiossulfato na reação Na2S2O3(aq)+2 HCl(aq) !$ \rightarrow !$ 2 NaCl(aq)+ SO2(g)+H2O(!$ \ell !$)+S(s)
II – O dióxido de manganês atua como agente oxidante do cloreto na reação MnO2(s) + 4 HCl(aq) !$ \rightarrow !$ MnCl2(aq) + Cl2(g) + 2 H2O(!$ \ell !$)
III – O carbonato de cálcio é oxidado pelo ácido clorídrico na reação CaCO3 (s) + 2 HCl(aq) !$ \rightarrow !$ CaCl2 (aq) + CO2(g) + H2O(!$ \ell !$)
IV – O zinco metálico é oxidado pelo ácido clorídrico na reação Zn(s) + 2 HCl(aq) !$ \rightarrow !$ ZnCl2(aq) + H2(g)
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
O peróxido de hidrogênio, sob o ponto de vista de reações de oxidação e redução, é um composto bastante versátil já que pode atuar como agente redutor ou oxidante. A reação entre soluções de peróxido de hidrogênio e de dicromato de potássio em meio ácido pode ser utilizada para caracterização do peróxido de hidrogênio.
O teste envolve a observação do composto CrO5 em fase orgânica, uma vez que esse composto é altamente instável em meio aquoso. Caso o solvente orgânico não seja adicionado, observam-se a coloração característica dos íons cromo III e a liberação de gás oxigênio.
A equação devidamente balanceada da reação entre as soluções de peróxido de hidrogênio e de dicromato de potássio em meio ácido, sem adição de solvente orgânico, é
Provas
Questão presente nas seguintes provas
O gráfico abaixo mostra a variação nos valores da 1ª à 5ª Energia de Ionização (EI) de três elementos (M, X e Z) de um mesmo período da tabela periódica.
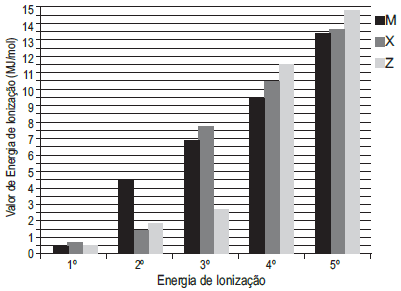
Analisando o gráfico, verifica-se que
Provas
Questão presente nas seguintes provas
Os catalisadores são amplamente empregados no refino de petróleo. Com relação a essas substâncias, analise as afirmações a seguir.
I – Os catalisadores aumentam a velocidade da reação, pois diminuem a energia de ativação da mesma.
II – A presença de catalisadores não influencia na variação de entalpia da reação química.
III – A presença de um catalisador altera o valor da constante de equilíbrio da reação.
IV – O emprego de níquel sólido na redução de alquenos é um exemplo de catálise heterogênea.
Estão corretas APENAS as afirmações
Provas
Questão presente nas seguintes provas
O tratamento de água para consumo humano segue uma série de procedimentos físico-químicos para remoção de impurezas. Ao final desses processos, a água apresenta pH em torno de 4,5. A última etapa do tratamento faz a correção do pH para diminuir a acidez da água. Para fazer essa correção no pH da água, deve ser utilizado o
Provas
Questão presente nas seguintes provas
Considere a pilha, representada pelo diagrama abaixo.
Cu(s) | Cu2+(aq, 1,0 mol/L) || Cl−1(aq, 1,0 mol/L) | Cl2(g, 1,0 atm) | Pt(s)
Dados os potenciais padrões de redução:
!$ ε !$0[Cu2+(aq)/Cu(s)] = +0,34V
!$ ε !$0[Cl2(g)/Cl−(aq)] = +1,36V
No processo eletroquímico em questão, a(o)
Provas
Questão presente nas seguintes provas
Com relação à eletrólise de uma solução aquosa de iodeto de sódio (NaI), empregando eletrodos inertes de grafite, analise as afirmativas a seguir.
I – Haverá formação de gás no polo negativo (catodo).
II – O pH da solução tende a diminuir em função da formação de íons H+ no anodo.
III – A concentração de íons I− tende a diminuir na solução.
IV – A concentração de íons Na+ tende a diminuir na solução.
Dados:
!$ ε !$0[Na+(aq)/Na(s)] = −2,71V
!$ ε !$0[H2O(l)/H2(g),OH−(aq)] = −0,83V
!$ ε !$0[I2(g)/I−(aq)] = +0,54 V
!$ ε !$0[O2(g), H+(aq)/H2O(l)] = +1,23V
Estão corretas APENAS as afirmativas
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container