Foram encontradas 100 questões.
Em estudo para se determinar a lei de velocidade da reação genérica A + B → C, foi utilizado o método das velocidades iniciais, tendo sido realizadas duas séries de reações. Na primeira série, utilizou-se sempre a mesma concentração inicial de B ([B]0) e variou-se a concentração inicial de A ([A]0). As velocidades iniciais foram medidas e plotadas em um gráfico contra [A]0, representado na Figura 1. Na segunda série, foi realizado procedimento semelhante, porém com a utilização da mesma [A]0 e variando-se [B]0, tendo sido obtido o gráfico representado na Figura 2.
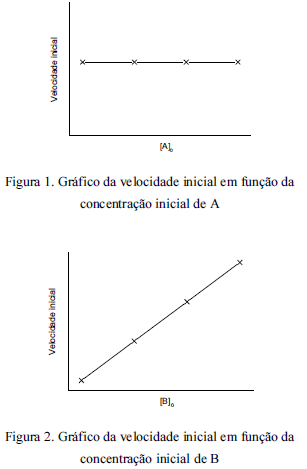
Com base no procedimento descrito, infere-se que a reação em tela é de ordem
Provas
Texto 8A1-II
O SO2Cl2 (g) decompõe-se facilmente de acordo com a equação:
!$ SO_2 Cl_2(g) \rightleftharpoons SO_2(g) + Cl_2(g)\,\,\,\triangle H>0 !$
Por esse motivo, ele é muito empregado como fonte de Cl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa reação apresentem comportamento ideal e que a lei de velocidade para a reação seja dada pela equação v = k × [SO2Cl2]. Considere também que, na temperatura em que a reação ocorre (T), a constante de equilíbrio (Keq) da reação valha 0,40.
Ainda considerando-se o texto 8A1-II, é correto afirmar que, do ponto de vista do equilíbrio químico, a decomposição do SO2Cl2 (g) é favorecida
Provas
Texto 8A1-II
O SO2Cl2 (g) decompõe-se facilmente de acordo com a equação:
!$ SO_2 Cl_2(g) \rightleftharpoons SO_2(g) + Cl_2(g)\,\,\,\triangle H>0 !$
Por esse motivo, ele é muito empregado como fonte de Cl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa reação apresentem comportamento ideal e que a lei de velocidade para a reação seja dada pela equação v = k × [SO2Cl2]. Considere também que, na temperatura em que a reação ocorre (T), a constante de equilíbrio (Keq) da reação valha 0,40.
De acordo com a reação apresentada no texto 8A1-II, o tempo de meia vida (t1/2) do SO2Cl2 (g), entendido como o período de tempo necessário para que a concentração da espécie caia à metade da concentração inicial, pode ser calculado por meio da expressão
Provas
Texto 8A1-II
O SO2Cl2 (g) decompõe-se facilmente de acordo com a equação:
!$ SO_2 Cl_2(g) \rightleftharpoons SO_2(g) + Cl_2(g)\,\,\,\triangle H>0 !$
Por esse motivo, ele é muito empregado como fonte de Cl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa reação apresentem comportamento ideal e que a lei de velocidade para a reação seja dada pela equação v = k × [SO2Cl2]. Considere também que, na temperatura em que a reação ocorre (T), a constante de equilíbrio (Keq) da reação valha 0,40.
Considerando-se as informações do texto 8A1-II, se, inicialmente, houver SO2Cl2 (g) à pressão parcial inicial de 1,50 bar em um sistema fechado isento de SO2 (g) e Cl2 (g), então a pressão parcial do SO2Cl2 (g), quando atingido o equilíbrio químico à temperatura T, será igual a
Provas
Em uma expansão isotérmica reversível, à temperatura T, de n mols de um gás ideal desde um volume inicial de 10 L até um volume final de 20 L, se R representa a constante universal dos gases, então a variação de entropia (!$ \triangle !$S) do sistema pode ser corretamente calculada por meio da expressão
Provas
Caso se deseje aquecer uma amostra de gás natural,
Provas
Um tanque foi carregado com determinada quantidade de gás natural comprimido à temperatura ambiente e, ao se medir a pressão no tanque, verificou-se que ela era consideravelmente menor que a esperada de acordo com a lei dos gases ideais para a temperatura em questão.
Nessa situação, o comportamento descrito deve-se
Provas
Texto 8A1-I
O metano, componente majoritário do gás natural, pode ser convertido, por meio de sua oxidação parcial, em gás de síntese, uma mistura de CO (g) e H2 (g), conforme a equação que se segue.
!$ CH_4(g) + ^1/_2 O_2 (g) \rightleftharpoons CO(g) + 2 H_2 (g) !$
As entalpias padrão de ligação (Hlig) envolvidas na reação são fornecidas na tabela a seguir.
| ligação | Hlig (kJ/mol) | ligação | Hlig (kJ/mol) |
| C—H | 412 | C≡O | 1.074 |
| O=O | 496 | H—H | 436 |
Com o emprego de catalisadores adequados, o gás de síntese pode ser convertido em uma variedade de produtos de grande interesse, como, por exemplo, combustíveis líquidos.
Na reação de obtenção de combustíveis líquidos a partir do gás de síntese, conforme mencionado no texto 8A1-I, o catalisador aumenta a velocidade de reação porque
Provas
Texto 8A1-I
O metano, componente majoritário do gás natural, pode ser convertido, por meio de sua oxidação parcial, em gás de síntese, uma mistura de CO (g) e H2 (g), conforme a equação que se segue.
!$ CH_4(g) + ^1/_2 O_2 (g) \rightleftharpoons CO(g) + 2 H_2 (g) !$
As entalpias padrão de ligação (Hlig) envolvidas na reação são fornecidas na tabela a seguir.
| ligação | Hlig (kJ/mol) | ligação | Hlig (kJ/mol) |
| C—H | 412 | C≡O | 1.074 |
| O=O | 496 | H—H | 436 |
Com o emprego de catalisadores adequados, o gás de síntese pode ser convertido em uma variedade de produtos de grande interesse, como, por exemplo, combustíveis líquidos.
Julgue os itens a seguir, considerando que, em um sistema fechado, esteja ocorrendo a reação de formação do gás de síntese a partir da oxidação parcial do CH4 (g), conforme descrita no texto 8A1-I, que, inicialmente, haja apenas CH4 (g) e O2 (g) no sistema e que, nas condições da reação, todas as espécies se comportem como gases ideais.
I A pressão parcial do CO (g), a qualquer momento, será igual à pressão parcial do CH4 (g).
II A pressão total, a qualquer momento, corresponde à média entre as pressões parciais de cada gás presente no sistema.
III A pressão parcial do H2 (g) será sempre superior à do CO (g).
Assinale a opção correta.
Provas
Texto 8A1-I
O metano, componente majoritário do gás natural, pode ser convertido, por meio de sua oxidação parcial, em gás de síntese, uma mistura de CO (g) e H2 (g), conforme a equação que se segue.
!$ CH_4(g) + ^1/_2 O_2 (g) \rightleftharpoons CO(g) + 2 H_2 (g) !$
As entalpias padrão de ligação (Hlig) envolvidas na reação são fornecidas na tabela a seguir.
| ligação | Hlig (kJ/mol) | ligação | Hlig (kJ/mol) |
| C—H | 412 | C≡O | 1.074 |
| O=O | 496 | H—H | 436 |
Com o emprego de catalisadores adequados, o gás de síntese pode ser convertido em uma variedade de produtos de grande interesse, como, por exemplo, combustíveis líquidos.
Com base nas entalpias padrão de ligação fornecidas no texto 8A1-I, é correto concluir que a entalpia padrão da reação de formação do gás de síntese a partir da oxidação parcial do CH4 (g) é igual a
Provas
Caderno Container