Foram encontradas 190 questões.
Em um recipiente fechado, são adicionados hidrogênio e nitrogênio, ambos no estado gasoso. No recipiente são ajustadas as condições para que o material reaja segundo a equação abaixo:
Keq
3H2(g) + N2(g) ⇄ 2NH3(g)
Depois de atingido o equilíbrio, a concentração de hidrogênio (H2(g)) é igual a 0,34 molL-1, e a de amônia (NH3(g)) é igual a 0,44 molL-1.
Dados: Keq = 6,1 mol-2L2
Qual a concentração de nitrogênio (N2(g)) no equilíbrio?
Provas
Algumas substâncias podem ser obtidas a partir de diferentes matérias-primas submetidas às mesmas condições.
O composto X, por exemplo, pode ser obtido a partir de um aldeído, um éster ou um ácido carboxílico, como representado na figura abaixo:
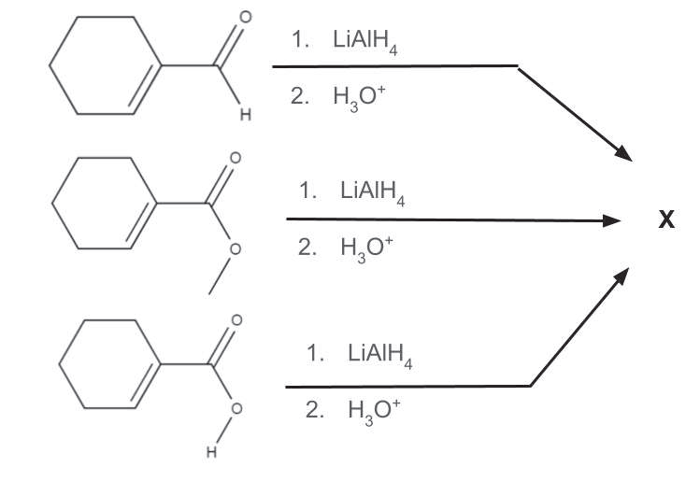
A alternativa que contém a representação estrutural do composto X é:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Um técnico necessita preparar uma solução contendo ácido clorídrico e ácido acético em mistura, com concentrações de 0,05 mol/L e 0,06 mol/L, respectivamente.
No laboratório, ele dispõe de água destilada e um balão volumétrico de 500 mL, além das demais vidrarias necessárias. No almoxarifado, ele dispõe de soluções cujos rótulos estão representados abaixo.

Dados:
Massa molar do ácido clorídrico: 36,5 g/mol
Massa molar do ácido acético: 60 g/mol
Qual das opções a seguir apresenta os volumes corretos de cada ácido que o técnico deve usar para que obtenha a solução de que precisa?
Provas
O brometo de pinavério, cuja estrutura está representada abaixo, tem efeitos antiespasmódicos no músculo liso gastrointestinal e pode aliviar os principais sintomas da síndrome do intestino irritável. Esse medicamento é comercializado em comprimidos contendo 100 mg do princípio ativo.
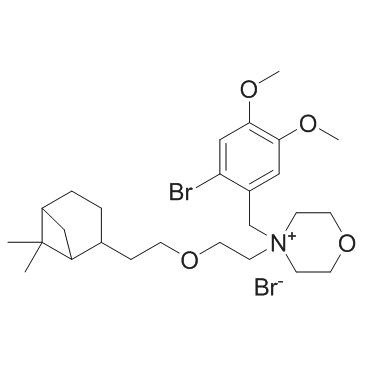
Um analista dissolve completamente um comprimido de brometo de pinavério obtendo 200 mL de solução, depois toma 50 mL desse material e trata com solução de nitrato de prata, gerando massa de brometo de prata que se precipita no recipiente.
BOR, Serhat et al. Efficacy of pinaverium bromide in the treatment of irritable bowel syndrome: a systematic review and meta-analysis. Therapeutic advances in gastroenterology, v. 14, p. 17562848211033740, 2021. (usado com adaptações).
Dados:
Massa molar do brometo de pinavério: 591 g/mol
Massa molar do brometo de prata: 188 g/mol
Desconsiderando possíveis interferentes e impurezas e considerando que o nitrato de prata está em excesso, qual das alternativas é a mais próxima da massa de brometo de prata que foi formada?
Provas
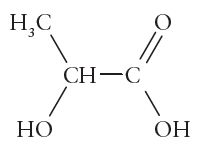
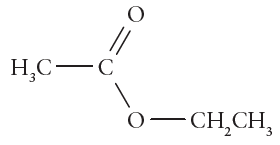
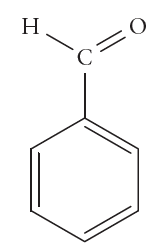
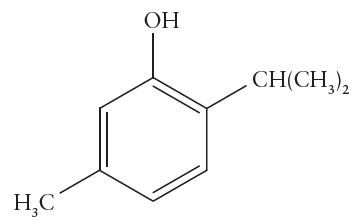
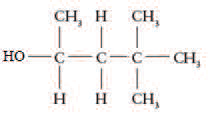
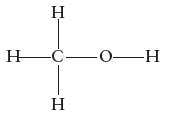
Nos procedimentos de lavagens de vidrarias de laboratório, é comum incluir uma etapa de enxágue com um solvente que elimine tinta de canetas ou outros componentes com baixa solubilidade em água. O técnico do laboratório de Química Geral costuma usar etanol 92% (álcool etílico) nesse processo, mas está sem o produto, pois as entregas das compras atrasaram. Contudo ele possui as seguintes opções com boas quantidades no almoxarifado:
| A | B | C |
|---|---|---|
|
|
|
| D | E | F |
|
|
|
| G | H | |
 |
|
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7 ed. Porto Alegre: Bookman, 2018. (material do professor, usado com adaptações)
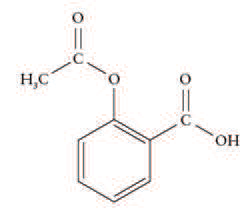
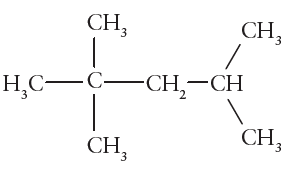
Querendo o técnico usar um composto similar, quais opções disponíveis no almoxarifado apresentam a mesma função orgânica e, portanto, poderiam ser consideradas para substituir o etanol de lavagem?
Provas
Um técnico preparou três compostos contendo enxofre e oxigênio em sua composição e mediu as massas de cada um desses elementos nesses compostos. Os resultados das massas estão apontados na tabela a seguir:

Considerando os dados acima, a fórmula que expressa a relação entre os átomos de S e O (desconsidere as cargas que eventualmente pode haver nos compostos) dos compostos 1, 2 e 3 é, respectivamente:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
| Frasco | Quantidade | Composição sugerida |
|---|---|---|
| 1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
| 2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
| 3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
A composição indicada nos rótulos aponta que o frasco 1 contém uma substância ácida, a solução do frasco 2 apresenta um sal neutro enquanto a solução do frasco 3 apresenta uma substância de caráter básico.
Dentre as alternativas, qual apresenta uma substância ácida, neutra e básica, respectivamente, de acordo com a teoria ácido-base de Bronsted?
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
| Frasco | Quantidade | Composição sugerida |
|---|---|---|
| 1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
| 2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
| 3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
O técnico separou 200 ml de cada frasco para analisar. Após análise, o frasco 3 indicou uma concentração de 4,3mol L-1 de KOH e a ausência de contaminantes, podendo apenas neutralizar e descartar a solução na pia. Dentre as opções disponíveis e menos dispendiosas, o técnico optou por um resíduo de HCl 1,5 mol L-1 que tinha sido gerado e que também precisava ser descartado.
Considerando os volumes e as concentrações apresentados, qual alternativa apresenta o volume mais próximo do necessário para neutralizar totalmente os 11 litros restantes da solução de KOH?
Provas
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
| Frasco | Quantidade | Composição sugerida |
|---|---|---|
| 1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
| 2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
| 3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
Uma das propriedades relevantes dessas soluções que deve ser confirmada é o pH, que indicaria se a solução é ácida, neutra ou básica, como se espera para os frascos 1, 2 e 3, respectivamente. Essa medida de acidez e basicidade pode ser feita, qualitativa ou quantitativamente, no laboratório de Química usando diferentes equipamentos, vidrarias e/ou reagentes.
Das alternativas abaixo, qual apresenta as três possibilidades adequadas para estimar o pH das soluções?
Provas
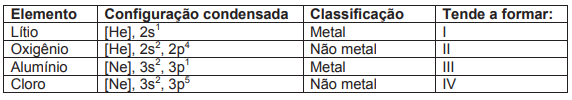
Os estudos em mecânica quântica possibilitaram a organização dos elétrons em orbitais, permitindo conhecer a configuração eletrônica de cada elemento químico representado na tabela periódica. Uma das aplicações dessa configuração é conhecer o número de elétrons na camada de valência, e, com isso, prever o número de elétrons envolvidos e/ou o tipo de ligação química que esse elemento tende a fazer.
Dessa forma, considerando os elementos abaixo, assinale a alternativa que apresente, em I, II, III e IV, os íons que cada elemento tende a formar.
Provas
Caderno Container