Foram encontradas 50 questões.
Considere a equação não-balanceada a seguir:
NiOOH(s) + Cl-(aq) \( \longrightarrow \) Ni(OH)2(s) + ClO-(aq)
Para o balanceamento correto dessa equação:
Provas
Cloreto de alumínio, AℓCℓ3, é um reagente barato usado em muitos processos industriais. Ele é obtido tratando-se sucatas de alumínio com cloro gasoso. Dados: N = 6,022 x 1023 mol-1, M (g.mol-1) Al = 26,98; Cl = 35,453.
1. Alumínio é o reagente limitante quando 5,40 g de alumínio são reagidos com 4,05 g de cloro gasoso.
2. Ao se reagir 12,3 g de alumínio são obtidos 47,44 g de AℓCℓ3 com rendimento de 78%.
3. Se 5% da sucata são impurezas, teoricamente 4,6 toneladas de AℓCℓ3 poderiam ser obtidos com 100% de rendimento, a partir de 1 tonelada de sucata.
4. 19,03 x 1023 moléculas de cloro gasoso são necessárias para se produzir 133,5 g de cloreto de alumínio.
Assinale a alternativa correta.
Provas
Qual é a massa de CaSO4.H2O 89% necessária para preparar 250 ml de uma solução 0,2 mol.L-1. Dados: M (g.mol-1) H = 1,008; O = 15,999; S = 32,066; Ca = 40, 078.
Provas
A análise de um composto orgânico forneceu as seguintes porcentagens dos seus componentes: C 44,4 %, H 6,2 % e O 49,4 %. Qual a fórmula empírica desse composto? Dados: M (g.mol-1) H = 1,008; C = 12,01; O = 15,999.
Provas
Para preparar 50 ml de uma solução tamponada de pH 7,5, qual das condições a seguir é a necessária?
Dados: NaH2PO4 pKa = 6,86; Na2HPO4 pKa = 12,4; M (g.mol-1) H = 1,008; O = 15,999; Na = 22,990; P = 30,974.
Provas
Numa titulação de 30 ml de um ácido fraco HA (Ka (25 ºC) = 1,34 x 10-5 mol.L-1), 0,1 mol.L-1 por NaOH 0,100 mol.L-1, o valor de pH no ponto onde [HA] = [A-] é:
Provas
Considere a reação entre piridina e água apresentada a seguir:
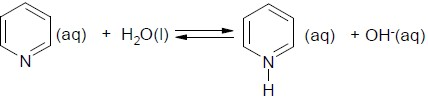
1. A piridina é uma base de Br⌀nsted-Lowry.
2. A piridina é uma base de Arrhenius.
3. A piridina é uma base fraca, pois é mais fraca que OH¯(aq).
4. OH¯(aq) é a base conjugada do ácido H2O.
Assinale a alternativa correta.
Provas
Com base na reação a seguir, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F).
LiH(s) + H2O(l) \( \longrightarrow \) Li+(aq) + OH-(aq) + H2(g)
( ) A reação descrita pela equação é de dupla troca.
( ) Nessa reação há mudança no NOX do lítio.
( ) É uma reação de oxirredução.
( ) O LiH tem caráter básico, pois ao dissolver torna o meio alcalino.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
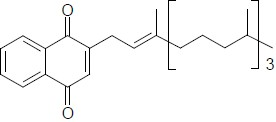
Numere a segunda coluna de acordo com sua correspondência com a primeira coluna.
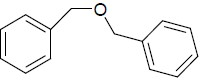
1. 
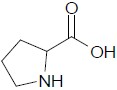
2. 
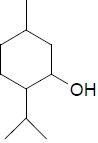
3. 
4. 
5. 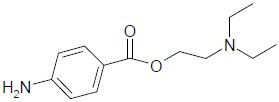
( ) Cetona.
( ) Álcool.
( ) Aminoácido.
( ) Éter.
( ) Éster.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
Provas
Numere a segunda coluna com base na informação da primeira coluna.
1. Aℓ2O3.
2. Mg(OH)2.
3. H2SO4.
4. Na2HPO4.
( ) Sal.
( ) Ácido.
( ) Óxido.
( ) Base.
Assinale a alternativa que apresenta a numeração correta da segunda coluna, de cima para baixo.
Provas
Caderno Container