Foram encontradas 40 questões.
Para uma aula experimental será necessário utilizar uma solução padronizada de ácido clorídrico 0,05 mol/L. Para a padronização, o técnico realizou a análise em triplicata utilizando as seguintes alíquotas de carbonato de sódio, como padrão primário: m1 = 0,0647 g; m2 = 0,0650 g; m3 = 0,0674 g. Considerando que foram gastos, em média, 23,40 mL da solução ácida na titulação, assinale a alternativa que apresenta a concentração real da solução de ácido clorídrico, expressa em mol/L.
Provas
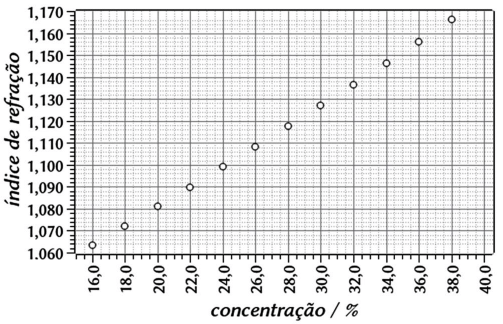
Um analista precisou verificar a concentração de uma solução aquosa de sacarose recentemente preparada. Para a verificação, estava disponível no laboratório um refratômetro de Abbae, e uma curva de calibração para soluções aquosas de sacarose, mostrada a seguir. A leitura do índice de refração da solução analisada apresentou valor de 1,104. Qual a concentração em % da solução de sacarose ?
Provas
Uma aula experimental aborda a verificação do ponto de equivalência da reação de uma solução aquosa de ácido sulfúrico 0,10 mol/L com uma solução aquosa de hidróxido de potássio 5% (m/V). O laboratório de química dispõe dos seguintes indicadores de pH (acompanhados dos valores de pH da zona de transição):
1. azul de timol (1,2 - 2,8)
2. amarelo de metila (2,9 - 4,0)
3. verde de bromocresol (4,0 - 5,6)
4. azul de bromotimol (6,0 - 7,6)
5. azul de timol (8,0 - 9,6)
Assinale a opção que correspondente ao indicador que deve ser utilizado no experimento descrito.
Provas
O processo de respiração celular é utilizado pela maioria dos seres vivos para obtenção de energia. Nesta reação, glicose e ácidos graxos são convertidos a CO2 e H2O, produzindo energia para outras funções do organismo, como indicado na equação química não balanceada abaixo:
C6H12O6 + O2 → CO2 + H2O
Tendo em vista que esta é uma reação de oxi-redução, assinale a alternativa que indica corretamente a semi-reação de oxidação da glicose.
Provas
As fermentações láctica e alcoólica são reações que alguns organismos vivos usam para obter energia em condições anaeróbias a partir da glicose, sendo que na primeira reação o produto é o ácido láctico (C3H6O3) e na segunda, etanol (CH3CH2OH) e CO2.
C6H12O6 → 2 C3H6O3 \( \Delta H \) = - 230 kJ (Fermentação láctica)
C6H12O6 → 2 CH3CH2OH + 2 CO2 \( \Delta H \) = - 230 kJ (Fermentação Alcoólica)
Sabendo-se que a reação de combustão completa do etanol é:
CH3CH2OH + 3 O2 → 2 CO2 + 3 H2O \( \Delta H \) = - 1.325 kJ
Deduz-se que a combustão completa de 1 mol de ácido lático:
Provas
Os air-bags de automóveis inflam devido à produção de N2 pelo contato entre azida de sódio (NaN3) e óxido férrico, no momento da colisão do veículo. O processo pode ser representado pela seguinte equação, não balanceada:
NaN3 + Fe2O3 → Na2O + Fe + N2
De acordo com as informações apresentadas, é correto afirmar que:
Provas
Equipamentos modernos de medida de pH (pH-metro) corrigem automaticamente a temperatura da solução problema para 25°C, através de um sensor acoplado ao equipamento. Porém alguns equipamentos portáteis mais antigos não ajustam o pH à temperatura. Neste caso qual leitura deverá ser obtida para uma amostra de água quimicamente pura a 40°C? (Dados: pKw = 14,00 (25°C) e pKw = 13,53 (40°C))
Provas
Pilhas alcalinas do tipo Ni/Cd são muito utilizadas atualmente devido a sua longa vida útil, altas correntes de trabalho e capacidade de recarga. Este tipo de bateria é constituído por um ânodo de liga de cádmio e cátodo de hidróxido básico de níquel, imersos em solução aquosa de KOH, que apresentam as seguintes semi-reações de redução:
Cd(OH)2 + 2e- → Cd + 2 OH- E0 = - 0,82 V
2 NiOOH + 4 H2O + 2e- → 2 Ni(OH)2.H2O + 2 OH- E0 = + 0,52 V
De acordo com os dados acima, assinale a alternativa que indica o potencial padrão da pilha de Ni/Cd.
Provas
Existem vários solventes que apresentam comportamento anfiprótico, isto é, exibem auto ionização tal como a água. Alguns destes solventes são listados no quadro abaixo:
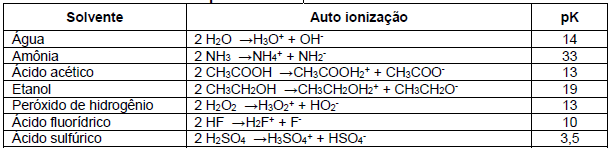
De acordo com os dados do quadro apresentado, em 1 mol das substâncias citadas é correto afirmar que:
Provas
Diversos compostos orgânicos são conhecidos por sua utilização como flavorizantes. Por serem capazes de conferir sabor e/ou aroma característico, são utilizados em pequenas quantidades como aditivos em alimentos e medicamentos. Um exemplo é o composto orgânico que apresenta aroma de abacaxi e pode ser sintetizado a partir da reação entre o ácido butanoico e o álcool etílico, na presença de um catalisador. A fórmula molecular do composto orgânico responsável pelo aroma de abacaxi é:
Provas
Caderno Container