Foram encontradas 13.430 questões.
Hidrociclones são empregados, principalmente, na concentração de suspensões sólido-líquido. Considerando uma suspensão em que a densidade do sólido é maior que a densidade do líquido, para aumentar a eficiência global de coleta do hidrociclone, deve-se
I – aumentar a densidade do líquido que constitui a suspensão.
II – aumentar a temperatura da suspensão.
III – adicionar chicanas no interior do hidrociclone.
IV – aumentar o tamanho das partículas presentes na suspensão alimentada ao hidrociclone.
V – diminuir a vazão que alimenta o hidrociclone.
É(São) correta(s) APENAS a(s) afirmativa(s)
Provas
Dados: densidade = 1,18 g cm-3, teor = 97 %.
O volume de ácido sulfúrico P.A. necessário para preparar 1,5 L de solução 2 mol L-1, em mL, é
Provas
Provas
Uma empresa realizará uma eleição para constituir os novos integrantes de sua Comissão Interna de Prevenção de Acidentes (CIPA). Quanto a essa situação, à luz da Norma Regulamentadora nº 5 do Ministério do Trabalho e Emprego (NR 5), é CORRETO afirmar que
Provas
Em química analítica, uma das maneiras de escolha dos métodos de análise está baseada na dimensão da amostra e nos níveis dos constituintes.
Sobre as técnicas de amostragem, analise estas afirmações.
I – A amostragem é o processo pelo qual uma amostra da população é reduzida em tamanho para uma quantidade de material homogêneo que pode ser manuseado no laboratório e cuja composição seja representativa da população.
II – Em relação à dimensão da amostra, o analito pode ser classificado nas escalas macro, semimicro, micro e ultramicro.
III – Na classificação dos tipos dos constituintes pelo nível do analito, os constituintes traço são aqueles presentes em quantidade entre 100 ppm (0,01%) e 1 ppb.
IV – A semimicroanálise é realizada com uma amostra na faixa de 0,001 a 0,01g.
Logo, pode-se dizer que são verdadeiras as seguintes afirmativas:
Provas
Nas sociedades indígenas, a pintura corporal tem grande importância. A tinta de cor vermelha é preparada com urucu, cujas sementes contêm aproximadamente 5% de pigmentos, com 70% a 80% de bixina, de fórmula molecular C25H30O4 e fórmula estrutural representada abaixo.
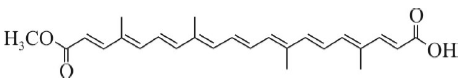
Para a preparação da tinta, as sementes de urucu, colhidas em maio e junho, são raladas em peneiras finas e fervidas em água, para formarem uma pasta, com a qual são feitas bolas, que, envolvidas em folhas, são guardadas durante todo o ano para serem usadas nas cerimônias de tatuagem.
Internet: <www.sbq.org.br> (com adaptações).
Tendo como referência o texto acima e as fórmulas da bixina, julgue os seguintes itens.
Considerando-se as massas atômicas 1,0 u, 12,0 u e 16 u para o hidrogênio, carbono e oxigênio, respectivamente, é correto afirmar que a massa contida em um mol de bixina é igual a 394 g.
Provas
O corpo humano utiliza a energia extraída dos alimentos, para manter o funcionamento dos seus órgãos, realizar seus processos bioquímicos, manter a temperatura do corpo e, ainda, realizar trabalhos externos, tais como andar, correr e pular.
A equação da conservação da energia no corpo humano é escrita como ) !$ \triangle\,E = \triangle\,Q - \triangle\,W !$, em que !$ \triangle\,E !$ a variação de energia interna ou, nesse contexto, da energia armazenada no corpo; !$ \triangle\,Q !$ é a quantidade de calor trocada com o ambiente e !$ \triangle\,W !$ é o trabalho realizado pelo corpo.
Quando em repouso, sem realizar trabalho externo, uma pessoa consome, em média, uma taxa de energia entre 100 W e 120 W. A taxa mínima de consumo, denominada taxa de metabolismo basal, indica a quantidade de energia necessária para a realização de tarefas imprescindíveis, tais como respiração e bombeamento de sangue através do sistema circulatório.
A energia utilizada pelo corpo é obtida a partir de reações de oxidação, como a da glicose, apresentada a seguir.
!$ C_6H_{12}O_6(s) + 6O_2(g) \xrightarrow{oxidação} 6H_2O(l) + 6CO_2(g) + 686\,Kcal !$
Nessa reação química, são liberadas 686 kcal por mol de glicose. A quantidade exata de energia liberada por litro de oxigênio consumido depende da dieta adotada. Em uma dieta típica, a energia liberada por litro de O2 consumido é de 4,9 kcal.
A eficiência 0 com que um corpo realiza o trabalho externo !$ \triangle\,W_{ext} !$ é definida por !$ \eta = { \large \triangle\,W_{ext} \over \triangle\,E} !$, em que !$ \triangle\,E !$ é a energia consumida durante a realização desse trabalho. !$ \triangle\,W_{ext} !$ pode ser diretamente
medido, ao passo que !$ \triangle\,E !$ é medido com base na quantidade de oxigênio consumido pelo corpo durante a realização do trabalho.
A esse respeito, considere
• aceleração da gravidade: g = 10 m/s2;
• constante universal dos gases: R = 8,31 J/mol K;
• temperatura Kelvin: K = C + 273, em que C é a temperatura em graus Celsius;
• valor da caloria: 1 cal = 4,19 J.
Tendo como referência o texto acima; considerando que uma pessoa em repouso produz exatamente o que consome de energia; assumindo as condições normais de pressão e temperatura (CNPT); desprezando as perdas de energia por reações de oxidação inacabadas e considerando, ainda, que todos os gases envolvidos são ideais, julgue o item.
Considere que um atleta com M kg de massa, partindo do repouso, comece a correr com aceleração constante de a m/s2; que, enquanto corre, o atleta sofre a ação de uma força de resistência constante igual a R newtons; que toda a energia do atleta resulta da oxidação de gordura, a qual é representada pela expressão a seguir, em que E é a energia, em joules, liberada por mol de gordura.
!$ \mathbf{ C_3 H_5 O_3 (OC_4H_7)_3 + 18,5O_2 \rightarrow 15CO_2 + 13H_2O + E} !$
Supondo-se que a eficiência do atleta seja 0, então a expressão matemática que representa a quantidade de moles N de gás carbônico produzido pelo atleta até o tempo t, em segundos, transcorrido desde o momento em que ele iniciou a corrida, é !$ N = { \large 15at^2 \over 2} { \large Ma+R \over \eta\,E} !$.
Provas
O corpo humano utiliza a energia extraída dos alimentos, para manter o funcionamento dos seus órgãos, realizar seus processos bioquímicos, manter a temperatura do corpo e, ainda, realizar trabalhos externos, tais como andar, correr e pular.
A equação da conservação da energia no corpo humano é escrita como ) !$ \triangle\,E = \triangle\,Q - \triangle\,W !$, em que !$ \triangle\,E !$ a variação de energia interna ou, nesse contexto, da energia armazenada no corpo; !$ \triangle\,Q !$ é a quantidade de calor trocada com o ambiente e !$ \triangle\,W !$ é o trabalho realizado pelo corpo.
Quando em repouso, sem realizar trabalho externo, uma pessoa consome, em média, uma taxa de energia entre 100 W e 120 W. A taxa mínima de consumo, denominada taxa de metabolismo basal, indica a quantidade de energia necessária para a realização de tarefas imprescindíveis, tais como respiração e bombeamento de sangue através do sistema circulatório.
A energia utilizada pelo corpo é obtida a partir de reações de oxidação, como a da glicose, apresentada a seguir.
!$ C_6H_{12}O_6(s) + 6O_2(g) \xrightarrow{oxidação} 6H_2O(l) + 6CO_2(g) + 686\,Kcal !$
Nessa reação química, são liberadas 686 kcal por mol de glicose. A quantidade exata de energia liberada por litro de oxigênio consumido depende da dieta adotada. Em uma dieta típica, a energia liberada por litro de O2 consumido é de 4,9 kcal.
A eficiência 0 com que um corpo realiza o trabalho externo !$ \triangle\,W_{ext} !$ é definida por !$ \eta = { \large \triangle\,W_{ext} \over \triangle\,E} !$, em que !$ \triangle\,E !$ é a energia consumida durante a realização desse trabalho. !$ \triangle\,W_{ext} !$ pode ser diretamente
medido, ao passo que !$ \triangle\,E !$ é medido com base na quantidade de oxigênio consumido pelo corpo durante a realização do trabalho.
A esse respeito, considere
• aceleração da gravidade: g = 10 m/s2;
• constante universal dos gases: R = 8,31 J/mol K;
• temperatura Kelvin: K = C + 273, em que C é a temperatura em graus Celsius;
• valor da caloria: 1 cal = 4,19 J.
Tendo como referência o texto acima; considerando que uma pessoa em repouso produz exatamente o que consome de energia; assumindo as condições normais de pressão e temperatura (CNPT); desprezando as perdas de energia por reações de oxidação inacabadas e considerando, ainda, que todos os gases envolvidos são ideais, julgue o item.
Se, em repouso, uma pessoa consome 0,34 L de oxigênio por minuto, então o aumento da temperatura do ar resultará em massa menor de oxigênio consumido por minuto pela pessoa, o que explica o fato de ser mais difícil se respirar em dias muito quentes.
Provas
O corpo humano utiliza a energia extraída dos alimentos, para manter o funcionamento dos seus órgãos, realizar seus processos bioquímicos, manter a temperatura do corpo e, ainda, realizar trabalhos externos, tais como andar, correr e pular.
A equação da conservação da energia no corpo humano é escrita como ) !$ \triangle\,E = \triangle\,Q - \triangle\,W !$, em que !$ \triangle\,E !$ a variação de energia interna ou, nesse contexto, da energia armazenada no corpo; !$ \triangle\,Q !$ é a quantidade de calor trocada com o ambiente e !$ \triangle\,W !$ é o trabalho realizado pelo corpo.
Quando em repouso, sem realizar trabalho externo, uma pessoa consome, em média, uma taxa de energia entre 100 W e 120 W. A taxa mínima de consumo, denominada taxa de metabolismo basal, indica a quantidade de energia necessária para a realização de tarefas imprescindíveis, tais como respiração e bombeamento de sangue através do sistema circulatório.
A energia utilizada pelo corpo é obtida a partir de reações de oxidação, como a da glicose, apresentada a seguir.
!$ C_6H_{12}O_6(s) + 6º_2(g) \xrightarrow{oxidação} 6H_2O(l) + 6CO_2(g) + 686\,Kcal !$
Nessa reação química, são liberadas 686 kcal por mol de glicose. A quantidade exata de energia liberada por litro de oxigênio consumido depende da dieta adotada. Em uma dieta típica, a energia liberada por litro de O2 consumido é de 4,9 kcal.
A eficiência 0 com que um corpo realiza o trabalho externo !$ \triangle\,W_{ext} !$ é definida por !$ \eta = { \large \triangle\,W_{ext} \over \triangle\,E} !$, em que !$ \triangle\,E !$ é a energia consumida durante a realização desse trabalho. !$ \triangle\,W_{ext} !$ pode ser diretamente
medido, ao passo que !$ \triangle\,E !$ é medido com base na quantidade de oxigênio consumido pelo corpo durante a realização do trabalho.
A esse respeito, considere
• aceleração da gravidade: g = 10 m/s2;
• constante universal dos gases: R = 8,31 J/mol K;
• temperatura Kelvin: K = C + 273, em que C é a temperatura em graus Celsius;
• valor da caloria: 1 cal = 4,19 J.
Tendo como referência o texto acima; considerando que uma pessoa em repouso produz exatamente o que consome de energia; assumindo as condições normais de pressão e temperatura (CNPT); desprezando as perdas de energia por reações de oxidação inacabadas e considerando, ainda, que todos os gases envolvidos são ideais, julgue o item.
Dado que glicose e sacarose (C12H22O11) são solutos não eletrólitos e não voláteis, iguais quantidades, em mol, dissolvidos em mesma quantidade de água causam, qualitativamente e quantitativamente, os mesmos efeitos tonoscópicos e ebulioscópicos nessas soluções.
Provas
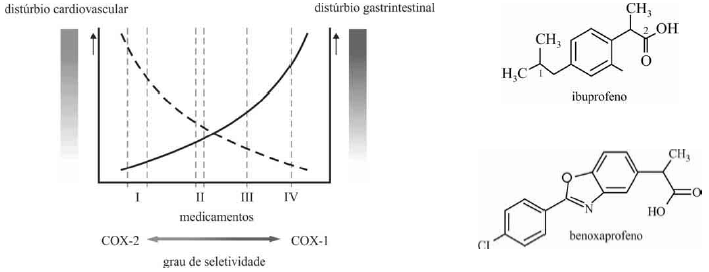
Na figura acima, são apresentadas duas curvas que relacionam o grau de seletividade de medicamentos com o distúrbio cardiovascular e o distúrbio gastrintestinal. Considere que, na figura, os medicamentos numerados de I a IV são indicados para o tratamento de inflamação na cavidade oral. Com base nessas informações, julgue o item.
A massa molar da fórmula molecular mínima do ibuprofeno é 220,0 g/mol.
Provas
Caderno Container