Foram encontradas 2.327 questões.
A combinação das Leis de Boyle, de Charles e de Avogadro gerou a Lei dos Gases Ideais, representada pela expressão PV = nRT. Essa é uma equação de estado que descreve a resposta de um gás ideal a mudanças de pressão, volume, temperatura e quantidade de moléculas. Entretanto, vários processos industriais e pesquisas em laboratório usam gases sob alta pressão ou em condições muito baixas de temperatura, condições às quais as leis dos gases ideais não são exatamente obedecidas. Nesses casos, o comportamento se assemelha ao dos gases reais. Em relação à teoria dos gases reais e ideais, afirma-se que
Provas
Questão presente nas seguintes provas
Soluções de permanganato de potássio utilizadas em titulações são frequentemente padronizadas por reação com ácido oxálico. Qual a relação molar de permanganato/ ácido oxálico dessa reação?
Provas
Questão presente nas seguintes provas
As principais funções químicas – ácidos, bases, sais e óxidos – são encontradas em nosso cotidiano e também em nosso organismo. As teorias definidas para estas funções químicas são citadas a seguir.
• Segundo a teoria de Arrhenius, “um ácido é todo composto molecular que, em solução aquosa, se ioniza, produzindo exclusivamente como cátion o H3O+ (hidroxônio) e que pode ser representado por H+”, e “uma base é um composto que em solução aquosa sofre dissociação iônica, produzindo íon hidroxila”.
• Segundo a teoria de Br⌀nsted-Lowry, “os ácidos são moléculas ou íons doadores de prótons” e “as bases são moléculas ou íons aceitadores de prótons”.
• Segundo a teoria de Lewis, “um ácido é um aceitador de par de elétrons”, e “uma base é um doador de par de elétrons”.
Com base nessas teorias, analise as afirmações abaixo.
I - HCl, HNO3, CH3COOH e CH4 são considerados ácidos, e NaOH, NH3 e KOH são considerados bases, segundo a teoria de Arrhenius.
II - HCl, HNO3, CH3COOH e CH4 são considerados ácidos, e NaOH, NH3 e KOH são considerados bases, segundo a teoria de Br⌀nsted-Lowry.
III - Na reação HCO3 − (aq) + NH4 + (aq) ⇔ H2CO3 (aq) + NH3 (aq), o íon amônio (NH4 + (aq)) e o ácido carbônico (H2CO3 (aq)) são considerados ácidos de Br⌀nsted-Lowry, e as espécies NH3 (aq) e HCO3 − (aq) são bases de Lewis.
Está correto APENAS o que se afirma em
Provas
Questão presente nas seguintes provas
Em relação às dispersões coloidais, afirma-se que
Provas
Questão presente nas seguintes provas
O abaixamento crioscópico do benzeno é utilizado na indústria do petróleo para medir massas molares de solutos. A equação que rege esse fenômeno pode ser expressa por:
!$ In(x_1)={large{Delta_fH over R}} left({large{1 over T_0}}-{large{1 over T}}
ight) !$
Sabe-se que:
• !$ x_1 !$ é a fração molar de solvente em solução que cristaliza na temperatura T;
• !$ Delta_f H !$ e !$ T_0 !$ são, respectivamente, a variação de entalpia e a temperatura de fusão do solvente puro;
• R é a constante universal dos gases que pode ser aproximada por 2 cal/(mol•K);
• a variação de entropia de fusão do benzeno puro é 8 cal/(mol•K);
• a massa molar do benzeno é 78 g/mol;
• a temperatura de fusão do benzeno (!$ T_0 !$) é 278,5 K.
A massa molar do soluto, a 278 K, necessária para a cristalização do benzeno a partir de uma solução de 10 g de soluto em 780 g de benzeno, em g/mol, é
Dado:!$ lim_{y
ightarrow 0} (In(1-y))cong -y !$
Provas
Questão presente nas seguintes provas
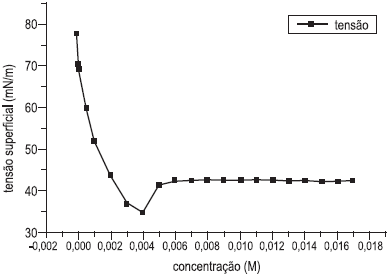
A figura acima apresenta dados experimentais de tensão superficial em função da concentração de surfactante (tenso-ativo) não iônico. Notam-se duas regiões distintas, uma de 0 a 0,003 M, e outra para concentrações acima de 0,005 M. A partir de uma análise, conclui-se que
Provas
Questão presente nas seguintes provas
Qual afirmação faz considerações corretas sobre o modelo de dupla camada elétrica de Gouy-Chapman?
Provas
Questão presente nas seguintes provas
Suponha que a temperatura de destilação de um determinado derivado do petróleo não possa ultrapassar 300 ºC. Três colunas de destilação, C1, C2 e C3, operam segundo uma distribuição normal com parâmetros apresentados na tabela a seguir.
| Coluna | Média |
Desvio
padrão
|
| C1 | 200 ºC | 50 ºC |
| C2 | 250 ºC | 80 ºC |
| C3 | 220 ºC | 100 ºC |
Sabendo-se que p1, p2 e p3 são as probabilidades de cada uma das colunas C1, C2 e C3, respectivamente, ultrapassar o limite máximo, conclui-se que
Provas
Questão presente nas seguintes provas
O tempo médio de permanência dos 600 empregados de uma empresa é de 5 anos com coeficiente de variação de 60%.
O Box-plot seguinte apresenta a distribuição do tempo de permanência.
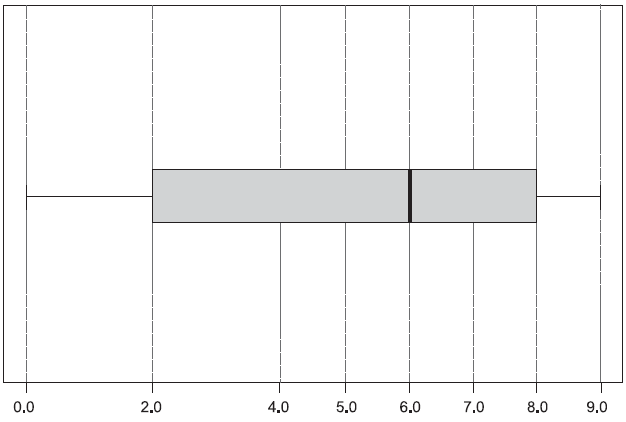
O número de empregados que permanecem na empresa entre 6 e 8 anos, e o desvio padrão para o tempo, em anos, de permanência são, respectivamente,
Provas
Questão presente nas seguintes provas
Analise as afirmativas a seguir sobre a transformada de Fourier, Tf(w), de uma função f(t) absolutamente integrável, real e de variável real.
I – Se f(t) for uma função par, a sua transformada Tf(w) será uma função real de variável real.
II – Se f(t) for uma função ímpar, a sua transformada Tf(w) será uma função real de variável real.
III – Se f(t) é uma função diferenciável tal que sua derivada é uma função absolutamente integrável, então Tf'(w)=wTf(w).
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container