Foram encontradas 505 questões.
O ar seco ao nível do mar é uma mistura gasosa composta
aproximadamente por 75,5% de N2 e 23,2% de O2 em massa
(porcentagem ponderal). Considerando-se que as massas molares
do N2 e do O2 são, respectivamente, 28,0 g/mol e 32,0 g/mol, e
considerando-se, ainda, a pressão total de 1,00 atm, é correto
afirmar que a pressão parcial do nitrogênio (N2) nessa mistura é
Provas
Questão presente nas seguintes provas
Gases reais desviam-se do comportamento ideal devido às
interações moleculares e ao volume ocupado pelas moléculas. A
equação de van der Waals utiliza constantes características para
cada gás. Sabendo que as constantes de van der Waals para o
argônio são a = 1,337 atm∙dm6
∙mol−2 (parâmetro que representa o
papel da atração) e b = 3,20 × 10−2 dm3
∙mol−1 (parâmetro que
representa o papel da repulsão), é correto concluir que a pressão
crítica (Pc) desse gás é
Provas
Questão presente nas seguintes provas
Em um experimento laboratorial, o ferro metálico reage com
ácido clorídrico produzindo hidrogênio gasoso e cloreto de
ferro(II) em solução aquosa. Nesse caso, considerando-se que o
ferro tenha massa molar de 55,85 g/mol, a quantidade de matéria
de gás hidrogênio produzida pela reação completa de 50,0 g de
ferro metálico com excesso de HCl é
Provas
Questão presente nas seguintes provas
A destilação fracionada utiliza sucessivos ciclos de vaporização e
condensação para separar componentes de uma mistura líquida
com diferentes volatilidades. Em relação a uma mistura que
forma um azeótropo de temperatura mínima de ebulição, é
correto afirmar que
Provas
Questão presente nas seguintes provas
As transições de fase em sólidos podem ser classificadas
conforme as variações nas funções termodinâmicas. Transições
em que a capacidade calorífica se torna infinita na temperatura de
transição são chamadas de transições λ. Um exemplo clássico de
transição de fase de segunda ordem (ou transição λ) que envolve
a modificação da simetria da estrutura cristalina sem
descontinuidade na entalpia é
Provas
Questão presente nas seguintes provas
No diagrama de fases da água, a inclinação da linha de equilíbrio
sólido-líquido é negativa. Isso significa que um aumento de
pressão pode provocar a fusão do gelo sem alteração de
temperatura. Do ponto de vista termodinâmico, essa característica
incomum da água é atribuída ao fato de que
Provas
Questão presente nas seguintes provas
As propriedades físicas dos líquidos, como o ponto de ebulição e
a entalpia de vaporização, refletem a intensidade das forças
intermoleculares. A regra de Trouton observa que a maioria dos
líquidos possui uma entropia de vaporização próxima a
85 J∙K−1∙mol−1. O desvio positivo significativo da água em
relação à regra de Trouton 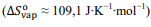 ocorre
devido
ocorre
devido
Provas
Questão presente nas seguintes provas
A teoria da repulsão por pares de elétrons da camada de valência
(VSEPR) permite prever a forma das moléculas com base na
repulsão eletrostática entre os pares de elétrons ao redor de um
átomo central. Nesse contexto, a geometria molecular e o ângulo
de ligação experimental de aproximadamente 107° da molécula
de amônia (NH3) são explicados
Provas
Questão presente nas seguintes provas
A estequiometria baseia-se em leis ou princípios empíricos que
descrevem como as massas das substâncias se combinam. Uma
dessas leis (ou princípio) afirma que volumes iguais de gases,
nas mesmas condições de temperatura e pressão, contêm o
mesmo número de moléculas, independentemente do gás. Essa
lei refere-se ao conceito fundamental conhecido como
Provas
Questão presente nas seguintes provas
O desenvolvimento da química como ciência quantitativa
fundamentou-se na observação experimental de que a energia e a
matéria não podem ser criadas nem destruídas, princípio
consolidado no final do século XVIII. Acerca do nascimento da
química moderna e da lei de conservação da massa, assinale a
opção correta.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container