Foram encontradas 120 questões.
J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
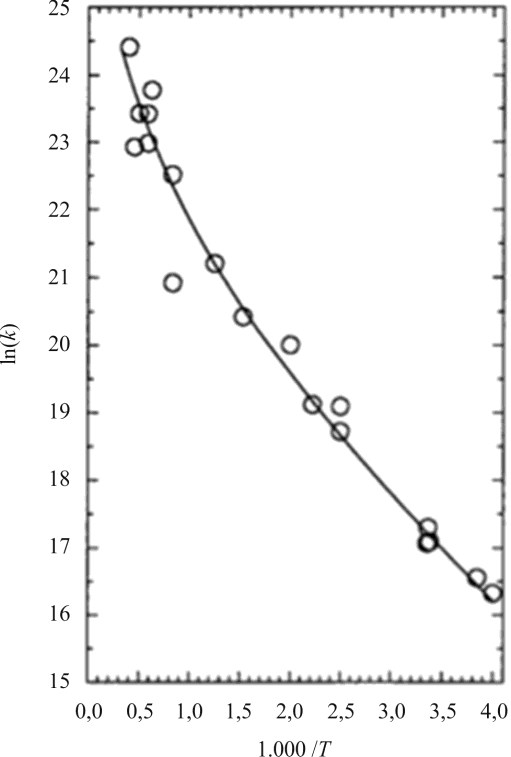
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Nos resultados experimentais apresentados no gráfico, a constante de velocidade k obedece à lei usual de Arrhenius em toda a faixa de temperaturas do experimento.
Provas

J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Pela teoria usual de Arrhenius, a energia de ativação de uma reação química é constante, mas, segundo a teoria de Aquilanti-Mundim, ela varia com a temperatura.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
O valor do potencial-padrão da célula eletroquímica em questão é menor que 0,3 V.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
A variação da energia livre de Gibbs-padrão (\( \Delta Gº \)) para a reação em apreço é negativa, com valor inferior a −45 kJ/mol, o que indica que a reação é espontânea nas condições-padrão.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
A constante de equilíbrio K para a reação em tela é da ordem de 107, o que indica que o equilíbrio é fortemente deslocado para a formação dos produtos (Fe3+ e I−).
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
Considerando-se a reação em comento, se o sistema em equilíbrio for perturbado por um aumento na concentração de I2, o equilíbrio se deslocará para a direita, no sentido de formação de Fe3+ e I−.
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A entropia de Boltzmann-Gibbs é definida por SBG = kBlnΩ, em que Ω representa o número de microestados acessíveis de um sistema fechado e kB, uma constante de proporcionalidade. Para sistemas independentes A e B, o número de microestados do sistema combinado fatoriza da seguinte forma: ΩA + B = ΩAΩ B . Em 1988, Tsallis propôs uma generalização, a entropia de Tsallis (Sq), que, para sistemas independentes, satisfaz Sq(A + B) = Sq(A) + Sq(B) + (1 − q) Sq(A)Sq(B), com q real. Com base nessas informações e nas leis da termodinâmica química, julgue os seguintes itens.
Considerando-se a entropia de Tsallis, caso os sistemas A e B sejam colocados em contato, a entropia do sistema final (A + B) não será aditiva, independentemente do valor do parâmetro q.
Provas
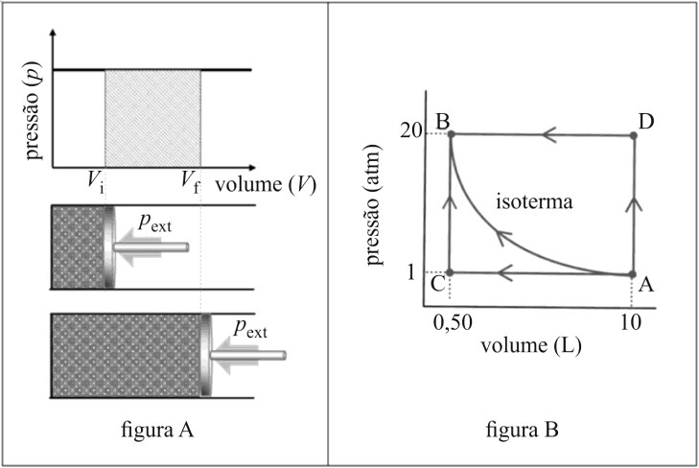
A figura (A) representa uma expansão de um gás ideal contra pressão externa constante (pext). A área hachurada no gráfico da figura (A) corresponde ao módulo do trabalho realizado pelo sistema sobre a vizinhança. A figura (B) mostra um gráfico de pressão (p) versus volume (V) desse mesmo gás, em condições isotérmicas. Com referência à situação ilustrada nas figuras (A) e (B), assumindo que os gases nelas retratados se comportem de forma ideal, que a temperatura na isoterma AB seja TA = TB = 313 K, que a constante dos gases seja R = 0,082 atm∙L∙K−1∙mol−1, que 1 L∙atm = 101 J e que ln(20) = 3, julgue os itens a seguir.
Contra pext constante, a variação de energia interna do gás será nula se a expansão for isotérmica.
Provas

A figura (A) representa uma expansão de um gás ideal contra pressão externa constante (pext). A área hachurada no gráfico da figura (A) corresponde ao módulo do trabalho realizado pelo sistema sobre a vizinhança. A figura (B) mostra um gráfico de pressão (p) versus volume (V) desse mesmo gás, em condições isotérmicas. Com referência à situação ilustrada nas figuras (A) e (B), assumindo que os gases nelas retratados se comportem de forma ideal, que a temperatura na isoterma AB seja TA = TB = 313 K, que a constante dos gases seja R = 0,082 atm∙L∙K−1∙mol−1, que 1 L∙atm = 101 J e que ln(20) = 3, julgue os itens a seguir.
A quantidade de matéria de gás no sistema descrito e seu volume nos estados B e C são, respectivamente, inferiores a 0,4 mol e 0,5 L.
Provas

A figura (A) representa uma expansão de um gás ideal contra pressão externa constante (pext). A área hachurada no gráfico da figura (A) corresponde ao módulo do trabalho realizado pelo sistema sobre a vizinhança. A figura (B) mostra um gráfico de pressão (p) versus volume (V) desse mesmo gás, em condições isotérmicas. Com referência à situação ilustrada nas figuras (A) e (B), assumindo que os gases nelas retratados se comportem de forma ideal, que a temperatura na isoterma AB seja TA = TB = 313 K, que a constante dos gases seja R = 0,082 atm∙L∙K−1∙mol−1, que 1 L∙atm = 101 J e que ln(20) = 3, julgue os itens a seguir.
Os trabalhos realizados sobre o gás ao longo dos caminhos ACB e ADB são iguais a 9,5 atm∙L e 190 atm∙L, respectivamente.
Provas
Caderno Container