Foram encontradas 2.550 questões.
A corrosão causa grandes prejuízos devido à deterioração de estruturas metálicas, sendo seu efeito agravado, nas grandes metrópoles, pelo fenômeno da chuva ácida. Na corrosão de uma estrutura de ferro, pode-se considerar que, primeiramente, os átomos do metal sejam oxidados pelo oxigênio dissolvido na água, conforme a reação I abaixo:
2Fe(s) + O2(g) + 2H2O(\( \ell \)) → 2Fe2+(aq) + 4OH-(aq)
Na sequência, o Fe2+ pode ainda ser oxidado a Fe3+ para formar o Fe2O3.H2O, que se deposita na forma de ferrugem.
Os potenciais padrão de redução (E0) das semirreações envolvidas na reação I são fornecidos abaixo:
Fe2+(aq) + 2e- → Fe(s) E0 = -0,44 V
O2(g) + 2H2O(\( \ell \)) + 4e- → 4OH-(aq) E0 = +0,40 V
A equação de Nernst é \( E = E^0 - { \large 0,0592 \over n} . log Q \), em que E, E0, n e Q são o potencial elétrico, o potencial elétrico padrão, o número de mols de elétrons envolvidos na reação e o quociente reacional, respectivamente.
Considerando as informações acima fornecidas, comportamento ideal para todas as soluções e gases envolvidos e, ainda, que a redução de uma unidade no valor do pH da água corresponda a um decréscimo de dez vezes na atividade dos íons OH-, julgue o item a seguir.
A redução de uma unidade no pH da água ocasiona acréscimo de 0,20 V no potencial elétrico da reação I.
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
Se for realizada a volume constante, a reação de decomposição do N2O4(g) a N2O(g) absorverá mais calor do que se for realizada a pressão constante.
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
À temperatura de 25 ºC, a entropia padrão da reação de decomposição do N2O4(g) a N2O(g) será superior a \( 150 \ J.mol^{-1} . K^{-1} \).
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
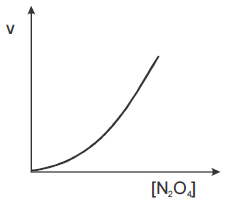
A figura abaixo representa a velocidade instantânea inicial (v) da reação de decomposição do N2O4(g) a NO2(g) em função da concentração do N2O4(g).
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
Durante a oxidação catalítica da amônia, o papel do catalisador é o de aumentar a taxa de colisão entre as moléculas dos reagentes, o que eleva a taxa de formação dos produtos.
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
Se, para uma mistura de N2O4(g) e NO2(g) em equilíbrio, for aumentado o espaço disponível para o gás ocupar, então, quando for atingido o equilíbrio novamente, a proporção do NO2 na mistura terá aumentado em relação à situação inicial.
Provas
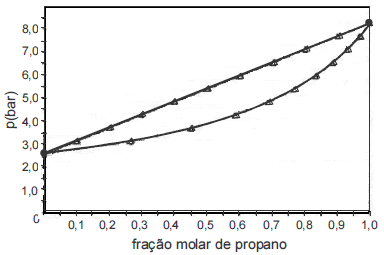
Considere que a figura acima represente o diagrama pressão-composição para a mistura propano-butano na temperatura de 293 K. Considere, ainda, que o propano e o butano formem uma mistura ideal e que o GLP apresente frações molares de butano e propano iguais a 0,30 e 0,70, respectivamente. A partir dessas informações, julgue o item a seguir.
No GLP sob pressão de 2,0 bar e temperatura de 20 ºC, as pressões parciais do butano e do propano são iguais a 0,6 bar e 1,4 bar, respectivamente.
Provas

Considere que a figura acima represente o diagrama pressão-composição para a mistura propano-butano na temperatura de 293 K. Considere, ainda, que o propano e o butano formem uma mistura ideal e que o GLP apresente frações molares de butano e propano iguais a 0,30 e 0,70, respectivamente. A partir dessas informações, julgue o item a seguir.
À temperatura de 20 ºC e sob pressão de 6,0 bar, uma mistura com a composição global do GLP apresentará duas fases: fase líquida, com fração molar de propano inferior a 0,70, e fase gasosa, com fração molar de propano superior a 0,70.
Provas
O gás natural (GN) e o gás liquefeito de petróleo (GLP) são largamente empregados como combustíveis. O principal componente do GN é o metano (CH4); já para o GLP, o principal componente é o propano (C3H8). Na tabela abaixo, são fornecidos parâmetros físico-químicos dessas substâncias.
| composto | metano | propano |
| \( ^1 \Delta H_c^0 (kJ ⋅ mol^{-1}) \) | -890 | -2.220 |
| \( ^2 S^0 (J ⋅ mol ^-1 ⋅ K^{-1}) \) | 186 | 270 |
| \( ^3C_{p,m} (J ⋅ mol^{-1} ⋅ K^{-1}) \) | 35,3 | 73,5 |
| \( ^4T_c (K) \) | 191 | 370 |
1entalplia padrão de combustão a 25 ºC
2entropia molar padrão a 25 ºC
3capacidade calorífica molar a pressão constante
4temperatura crítica
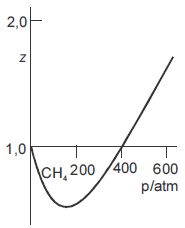
Na figura abaixo, é fornecida a curva do fator de compressibilidade (Z) do propano em função da pressão (p).
Com base nas informações acima, julgue o item a seguir.
De acordo com a terceira lei da termodinâmica, o propano, por apresentar maior massa molar, possui maior entropia molar que o metano no zero absoluto de temperatura.
Provas
O gás natural (GN) e o gás liquefeito de petróleo (GLP) são largamente empregados como combustíveis. O principal componente do GN é o metano (CH4); já para o GLP, o principal componente é o propano (C3H8). Na tabela abaixo, são fornecidos parâmetros físico-químicos dessas substâncias.
| composto | metano | propano |
| \( ^1 \Delta H_c^0 (kJ ⋅ mol^{-1}) \) | -890 | -2.220 |
| \( ^2 S^0 (J ⋅ mol ^-1 ⋅ K^{-1}) \) | 186 | 270 |
| \( ^3C_{p,m} (J ⋅ mol^{-1} ⋅ K^{-1}) \) | 35,3 | 73,5 |
| \( ^4T_c (K) \) | 191 | 370 |
1entalplia padrão de combustão a 25 ºC
2entropia molar padrão a 25 ºC
3capacidade calorífica molar a pressão constante
4temperatura crítica
Na figura abaixo, é fornecida a curva do fator de compressibilidade (Z) do propano em função da pressão (p).

Com base nas informações acima, julgue o item a seguir.
Considerando uma pressão constante igual a 1,0 bar, é correto afirmar que a quantidade de calor necessária para aquecer certa quantidade de metano de 25 ºC a 125 ºC será superior à quantidade de calor liberada pela queima dessa mesma quantidade de metano.
Provas
Caderno Container