Foram encontradas 3.020 questões.
Durante o processo de fabricação de comprimidos, é
possível observar alterações físicas no estado sólido do
fármaco. Essas modificações induzidas por processo podem resultar de diversas interações e condições durante as
etapas de produção, desde a mistura dos componentes até
a obtenção do comprimido final. Sobre alterações físicas
induzidas por processo, é correto afirmar que:
Provas
Questão presente nas seguintes provas
Um determinado medicamento, cujo insumo farmacêutico ativo é classificado como classe II do sistema de classificação biofarmacêutica, está em redesenvolvimento tecnológico para atingir melhorias em seu perfil de dissolução.
A estratégia da alteração pós-registro é a alteração da rota
produtiva, alterando o processo de compressão direta para
granulação úmida em granulador de alto cisalhamento com
secagem em leito fluidizado. Considerando a natureza
desta alteração pós-registro, são requisitos para a mudança
os abaixo relacionados, EXCETO:
Provas
Questão presente nas seguintes provas
A técnica de cromatografia em camada delgada pode
ser utilizada para a identificação de fármacos e de suas
substâncias relacionadas. Sobre essa técnica, avalie se
são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I- o princípio da análise de cromatografia em camada delgada baseia-se no fato de que as moléculas sob investigação são transportadas pela fase móvel e se movem através da fase estacionária em taxas variáveis.
II- quanto menor for a afinidade da molécula sob investigação com a fase estacionária, maior será o seu deslocamento na placa cromatográfica.
III- quanto maior for a afinidade da molécula sob investigação com a fase estacionária, maior será o seu deslocamento na placa cromatográfica.
IV- a cromatografia de camada delgada é empregada apenas para análises qualitativas de fármacos e de suas substâncias relacionadas. Uma vez que as moléculas de interesse permanecem aderidas à fase estacionária, sua quantificação não é possível.
A ordem correta, de cima para baixo, é:
I- o princípio da análise de cromatografia em camada delgada baseia-se no fato de que as moléculas sob investigação são transportadas pela fase móvel e se movem através da fase estacionária em taxas variáveis.
II- quanto menor for a afinidade da molécula sob investigação com a fase estacionária, maior será o seu deslocamento na placa cromatográfica.
III- quanto maior for a afinidade da molécula sob investigação com a fase estacionária, maior será o seu deslocamento na placa cromatográfica.
IV- a cromatografia de camada delgada é empregada apenas para análises qualitativas de fármacos e de suas substâncias relacionadas. Uma vez que as moléculas de interesse permanecem aderidas à fase estacionária, sua quantificação não é possível.
A ordem correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
Sobre a técnica de difração de raios X para a caracterização de fármacos é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
Considere os resultados de estabilidade de um lote um dado medicamento apresentado nas tabelas abaixo e o
seguinte contexto de histórico de desenvolvimento:
a. O insumo farmacêutico ativo presente neste medicamento apresentou degradação por hidrólise e por oxidação em estudos anteriores de degradação forçada.
b. O insumo farmacêutico ativo é fotoestável.
c. O projeto visa o registro sanitário de um medicamento no Brasil.
d. A indústria que fará a manufatura deste medicamento dispõe de equipamentos de emblistamento em materiais termomoldáveis e não possui equipamentos para emblistamento em materiais formados a frio.
e. O método utilizado no estudo de estabilidade é uma técnica cromatográfica, com leitura por UV a 310 nm, e é indicativo de estabilidade.
Os resultados estão descritos na tabela abaixo:
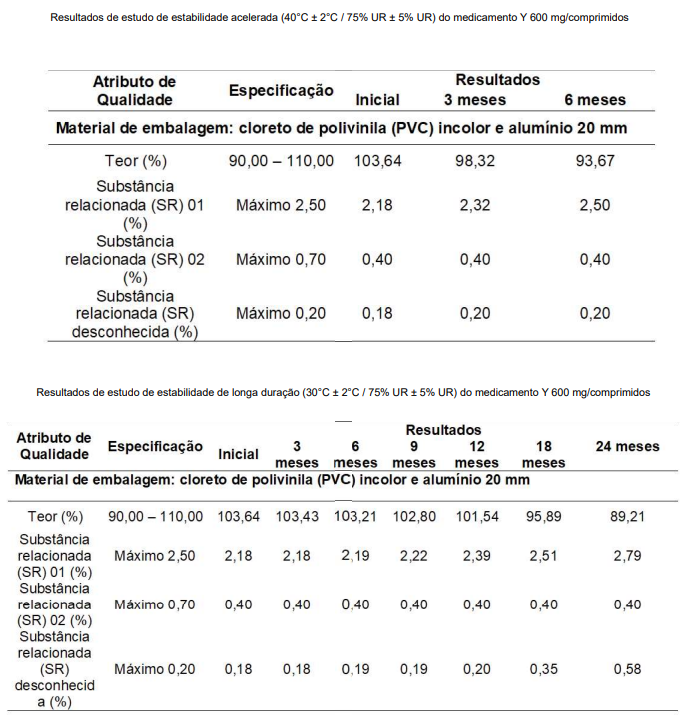
Com base nessas informações, avalie se são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I - O estudo de estabilidade apresentado pode, por si só, respaldar o pedido de prazo de validade de 24 meses para acondicionamento em temperatura ambiente.
II - O estudo de estabilidade acelerada está aprovado, uma vez que o teor do IFA e das substâncias relacionadas se mantém dentro dos limites especificados.
III - O estudo de estabilidade acelerada está reprovado e o de longa duração está aprovado até a frequência de 12 meses.
IV - Considerando o contexto histórico do desenvolvimento, blísteres formados com os materiais PVC âmbar ou policlorotrifluoretileno branco opaco (PCTFE) e selados com lâmina de alumínio 0,20 mm são boas alternativas para obter melhores resultados de estabilidade deste medicamento.
V - Considerando o contexto histórico do desenvolvimento, o material multicamada cloreto de polivinila/polietileno/ cloreto de polivinilideno (PVC/PE/PVdC), é uma boa alternativa para obter melhores resultados de estabilidade deste medicamento.
VI - Considerando o contexto histórico do desenvolvimento, o material multicamada contendo poliamida orientada, alumínio e PVC (OPA/ALU/PVC) selado com lâmina de alumínio é uma boa alternativa para obter melhores resultados de estabilidade deste medicamento.
VII - Considerando a compatibilidade dos materiais de embalagem primária alternativos e a capacidade industrial instalada, os blísteres de PVC/PE/PVdC são mais adequados. Os blísteres de OPA/ALU/PVC requerem investimentos industriais.
A ordem correta, de cima para baixo, é:
a. O insumo farmacêutico ativo presente neste medicamento apresentou degradação por hidrólise e por oxidação em estudos anteriores de degradação forçada.
b. O insumo farmacêutico ativo é fotoestável.
c. O projeto visa o registro sanitário de um medicamento no Brasil.
d. A indústria que fará a manufatura deste medicamento dispõe de equipamentos de emblistamento em materiais termomoldáveis e não possui equipamentos para emblistamento em materiais formados a frio.
e. O método utilizado no estudo de estabilidade é uma técnica cromatográfica, com leitura por UV a 310 nm, e é indicativo de estabilidade.
Os resultados estão descritos na tabela abaixo:

Com base nessas informações, avalie se são verdadeiras (V) ou falsas (F) as afirmações a seguir:
I - O estudo de estabilidade apresentado pode, por si só, respaldar o pedido de prazo de validade de 24 meses para acondicionamento em temperatura ambiente.
II - O estudo de estabilidade acelerada está aprovado, uma vez que o teor do IFA e das substâncias relacionadas se mantém dentro dos limites especificados.
III - O estudo de estabilidade acelerada está reprovado e o de longa duração está aprovado até a frequência de 12 meses.
IV - Considerando o contexto histórico do desenvolvimento, blísteres formados com os materiais PVC âmbar ou policlorotrifluoretileno branco opaco (PCTFE) e selados com lâmina de alumínio 0,20 mm são boas alternativas para obter melhores resultados de estabilidade deste medicamento.
V - Considerando o contexto histórico do desenvolvimento, o material multicamada cloreto de polivinila/polietileno/ cloreto de polivinilideno (PVC/PE/PVdC), é uma boa alternativa para obter melhores resultados de estabilidade deste medicamento.
VI - Considerando o contexto histórico do desenvolvimento, o material multicamada contendo poliamida orientada, alumínio e PVC (OPA/ALU/PVC) selado com lâmina de alumínio é uma boa alternativa para obter melhores resultados de estabilidade deste medicamento.
VII - Considerando a compatibilidade dos materiais de embalagem primária alternativos e a capacidade industrial instalada, os blísteres de PVC/PE/PVdC são mais adequados. Os blísteres de OPA/ALU/PVC requerem investimentos industriais.
A ordem correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
No âmbito do desenvolvimento de medicamentos na
indústria farmacêutica, o objetivo a seguir que é enfatizado
pelo conceito de Quality by Design (QbD), que busca não
apenas atender aos requisitos regulatórios, mas também
promover a excelência na qualidade do produto, é:
Provas
Questão presente nas seguintes provas
A implementação do guia ICH Q12 exige uma estrutura
regulatória atualizada no setor farmacêutico com a inclusão
de informações relacionadas às condições estabelecidas
(ECs) nas submissões regulatórias, facilitando um aumento
da capacidade do setor de gerenciar a implementação
de mudanças na química, fabricação e controles (CMC)
de forma mais eficaz no âmbito do sistema de qualidade
farmacêutica. Observe as afirmativas a seguir sobre as ECs.
I – As ECs são consideradas necessárias para garantir a qualidade do produto e, portanto, exigiriam uma submissão regulatória se fossem alteradas após a aprovação.
II – Para produtos comerciais desenvolvidos usando a abordagem tradicional, a aplicação de ECs pode se basear em um entendimento limitado com base em análise retrospectiva de dados históricos.
III – As ECs para um processo de fabricação devem ser definidas com base no entendimento do produto e do processo, levando em conta todos os elementos relevantes da estratégia de controle.
IV - Os parâmetros de processo em que não se pode excluir razoavelmente um impacto na qualidade do produto não devem ser identificados como ECs.
V – A abordagem baseada no desempenho para estabelecimento das ECs se concentra no controle de resultados do processo (atributos, medições, respostas) em vez de entradas do processo (parâmetros do processo e atributos do material).
Das afirmativas acima, é correto afirmar que:
I – As ECs são consideradas necessárias para garantir a qualidade do produto e, portanto, exigiriam uma submissão regulatória se fossem alteradas após a aprovação.
II – Para produtos comerciais desenvolvidos usando a abordagem tradicional, a aplicação de ECs pode se basear em um entendimento limitado com base em análise retrospectiva de dados históricos.
III – As ECs para um processo de fabricação devem ser definidas com base no entendimento do produto e do processo, levando em conta todos os elementos relevantes da estratégia de controle.
IV - Os parâmetros de processo em que não se pode excluir razoavelmente um impacto na qualidade do produto não devem ser identificados como ECs.
V – A abordagem baseada no desempenho para estabelecimento das ECs se concentra no controle de resultados do processo (atributos, medições, respostas) em vez de entradas do processo (parâmetros do processo e atributos do material).
Das afirmativas acima, é correto afirmar que:
Provas
Questão presente nas seguintes provas
O guia de estudo de estabilidade Nº 28 de 2019 apresenta recomendações para o cumprimento regulatório para
a realização dos estudos de estabilidade. Neste sentido,
avalie se são verdadeiras (V) ou falsas (F) as afirmativas
a seguir sobre os testes a serem realizados no estudo de
estabilidade, de acordo com o tipo de forma farmacêutica.
I – A quantificação de antioxidantes e conservantes, se estiverem presentes na formulação, é necessária para qualquer tipo de forma farmacêutica.
II – Se a pureza enantiomérica for importante para a eficácia e segurança do medicamento, deve ser comprovado que não ocorre racemização durante o estudo de estabilidade para qualquer tipo de forma farmacêutica.
III – A forma cristalina do insumo farmacêutico ativo no medicamento deve ser avaliada durante o estudo de estabilidade para qualquer forma farmacêutica, como comprimidos, cápsulas, soluções e suspensões.
IV – No caso de comprimidos dispersíveis, deve-se avaliar a dissolução, desintegração, umidade, dureza e friabilidade, sendo recomendada uma especificação de não mais que dez minutos para a desintegração.
As afirmativas I, II, III e IV são respectivamente:
I – A quantificação de antioxidantes e conservantes, se estiverem presentes na formulação, é necessária para qualquer tipo de forma farmacêutica.
II – Se a pureza enantiomérica for importante para a eficácia e segurança do medicamento, deve ser comprovado que não ocorre racemização durante o estudo de estabilidade para qualquer tipo de forma farmacêutica.
III – A forma cristalina do insumo farmacêutico ativo no medicamento deve ser avaliada durante o estudo de estabilidade para qualquer forma farmacêutica, como comprimidos, cápsulas, soluções e suspensões.
IV – No caso de comprimidos dispersíveis, deve-se avaliar a dissolução, desintegração, umidade, dureza e friabilidade, sendo recomendada uma especificação de não mais que dez minutos para a desintegração.
As afirmativas I, II, III e IV são respectivamente:
Provas
Questão presente nas seguintes provas
A Instrução Normativa - IN nº 45, de 21 de Agosto de
2019, que dispõe sobre as boas práticas de fabricação
complementares a medicamentos experimentais, adota
diversas definições, sendo correto afirmar que:
Provas
Questão presente nas seguintes provas
Um produto farmacêutico foi desenvolvido pela abordagem de Quality by Design (QbD) contendo um insumo
farmacêutico ativo da classe II do sistema de classificação
biofarmacêutica. Diferentes formulações foram produzidas
e avaliadas quanto ao perfil de dissolução. Para garantir um
entendimento completo de todas as possíveis influências no
design space, uma avaliação completa dos riscos do processo de fabricação foi conduzida utilizando a ferramenta
Análise dos Efeitos dos Modos de Falha (FMEA). Sobre o
estudo em questão, avalie se são verdadeiras (V) ou falsas
(F) as afirmativas a seguir.
I – Uma questão de risco adequada para iniciar o processo de gerenciamento de riscos à qualidade é “quais são as variáveis críticas de entrada e processamento do produto que impactariam na qualidade do produto com base no design space?”.
II – Usando a ferramenta FMEA é possível calcular o número de prioridade de risco (RPN), sendo que o quanto maior o número resultante, mais crítica é a falha e, consequentemente, mais prioritária deve ser a ação.
III – Considerando o risco relacionado à etapa do processo de lubrificação, é plausível afirmar que a alteração na dissolução afetando o desempenho clínico é um modo de falha, e o tempo de mistura muito longo é um efeito da falha.
IV – A dissolução é o atributo de qualidade relacionado no design space com as variáveis de processo.
As afirmativas I, II, III e IV são respectivamente:
I – Uma questão de risco adequada para iniciar o processo de gerenciamento de riscos à qualidade é “quais são as variáveis críticas de entrada e processamento do produto que impactariam na qualidade do produto com base no design space?”.
II – Usando a ferramenta FMEA é possível calcular o número de prioridade de risco (RPN), sendo que o quanto maior o número resultante, mais crítica é a falha e, consequentemente, mais prioritária deve ser a ação.
III – Considerando o risco relacionado à etapa do processo de lubrificação, é plausível afirmar que a alteração na dissolução afetando o desempenho clínico é um modo de falha, e o tempo de mistura muito longo é um efeito da falha.
IV – A dissolução é o atributo de qualidade relacionado no design space com as variáveis de processo.
As afirmativas I, II, III e IV são respectivamente:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container