Foram encontradas 3.300 questões.
Durante o processo de polimerização do poli(óxido de
etileno) são geradas moléculas de polímeros que apresentam
extremidades pouco reativas, dificultando assim o processo
de conjugação. Para facilitar a ligação do polímero à proteína
será necessário ativar o mesmo com um grupo reativo em
uma das extremidades. Dos grupamentos apresentados
abaixo, o único que não pode ser utilizado para ativar um
polímero que será conjugado a resíduos de aminoácidos que
apresentam grupamento amino livre é:
Provas
Questão presente nas seguintes provas
Com relação ao vírus causador da Rubéola e Síndrome da
Rubéola Congênita, analise as afirmativas abaixo.
I. Pode ser propagado em diversos tipos de células de mamíferos in vitro.
II. A transmissão é realizada com auxílio de inseto vetor.
III. É um vírus grande, envelopado, com genoma DNA pertencente ao gênero Rubivirus.
Assinale:
I. Pode ser propagado em diversos tipos de células de mamíferos in vitro.
II. A transmissão é realizada com auxílio de inseto vetor.
III. É um vírus grande, envelopado, com genoma DNA pertencente ao gênero Rubivirus.
Assinale:
Provas
Questão presente nas seguintes provas
A Rede de Frio é o processo de armazenamento,
conservação, manipulação, distribuição e transporte dos
imunobiológicos do Programa Nacional de Imunizações, e
deve ter as condições adequadas de refrigeração desde o
laboratório produtor até o momento em que a vacina é
administrada mantendo sua eficácia. Sobre o
armazenamento das vacinas virais do calendário nacional de
vacinação de acordo com Programa Nacional de
Imunizações(PNI), analise as afirmativas a seguir.
I. As vacinas liofilizadas contra o sarampo, caxumba e rubéola (SRC) e a vacina de febre amarela, antes de reconstituídas, podem ser armazenadas em refrigerador entre +2 ºC e +8 ºC ou congeladas sob temperatura de –20 ºC .
II. A vacina oral contra poliomielite (VOP) deve ser armazenada sob temperatura de –20 ºC para preservar sua potência por 24 meses.
III. A vacina líquida de hepatite B deve ser armazenada em refrigerador entre +2 ºC e +8 ºC e não pode ser congelada.
Assinale:
I. As vacinas liofilizadas contra o sarampo, caxumba e rubéola (SRC) e a vacina de febre amarela, antes de reconstituídas, podem ser armazenadas em refrigerador entre +2 ºC e +8 ºC ou congeladas sob temperatura de –20 ºC .
II. A vacina oral contra poliomielite (VOP) deve ser armazenada sob temperatura de –20 ºC para preservar sua potência por 24 meses.
III. A vacina líquida de hepatite B deve ser armazenada em refrigerador entre +2 ºC e +8 ºC e não pode ser congelada.
Assinale:
Provas
Questão presente nas seguintes provas
Os marcadores moleculares incluem:
I. isoenzimas que permitem a identificação ou a diferenciação de organismos.
II. sequências de DNA codificadoras de enzimas-repórter, facilitando a avaliação da eficiência de transformação ou da função de sequências reguladoras de DNA.
III. genes capazes de conferir resistência a antibióticos.
Assinale:
I. isoenzimas que permitem a identificação ou a diferenciação de organismos.
II. sequências de DNA codificadoras de enzimas-repórter, facilitando a avaliação da eficiência de transformação ou da função de sequências reguladoras de DNA.
III. genes capazes de conferir resistência a antibióticos.
Assinale:
Provas
Questão presente nas seguintes provas
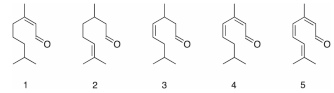
Dos monoterpenos abaixo. O que apresenta maior absorção
na espectroscopia no ultravioleta é:

Provas
Questão presente nas seguintes provas
Um aspecto essencial na validação de limpeza é determinar
quanto de limpeza é suficiente. Apesar de oficialmente não
endossar critérios adotados por indústrias farmacêuticas, o
FDA (Food Drug Administration) dos Estados Unidos da
América faz referência a critérios adotados pela empresa Eli
Lilly, que estabelece os seguintes critérios (LeBlanc, 1999):
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
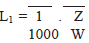
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
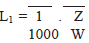
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
Provas
Questão presente nas seguintes provas
- Controle de QualidadeControle de Qualidade Industrial
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
No intuito de contribuir para o monitoramento da qualidade de medicamentos, a Agência Nacional de Vigilância Sanitária (ANVISA), em conjunto com o Instituto Nacional de Controle de Qualidade em Saúde, Fundação Oswaldo Cruz (INCQS/FIOCRUZ), instituiu o Programa Nacional de Verificação da Qualidade de Medicamentos (PROVEME). São critérios utilizados para a coleta de amostras para a verificação de qualidade:
I. medicamentos da rede SUS. II. medicamentos notificados com suspeitas de desvio da qualidade.
III. medicamentos de maior custo. IV. medicamentos analisados anteriormente que obtiveram resultado de análise insatisfatória.
Assinale:
Assinale:
Provas
Questão presente nas seguintes provas
A Instrução Normativa nº 5 de 11 de dezembro de 2008, em
seu anexo 1 discrimina a lista de espécies de registro
simplificado de fitoterápicos, constam nesta lista as seguintes
espécies:
Provas
Questão presente nas seguintes provas
- FarmacologiaFarmacologia e Pesquisa Clínica
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
sobre a condução de estudos envolvendo seres humanos,
com base nas normas locais, analise as opções abaixo.
I. A CONEP terá composição multi e transdisciplinar, com pessoas de ambos os sexos e deverá ser composta por 15 (quinze) membros titulares e seus respectivos suplentes.
II. Um dos documentos exigidos pela RDC 39/08 da ANVISA prevê o orçamento para a pesquisa. Este deve ser apresentado de forma detalhada prevendo recursos e especificando gastos com visitas médicas e de outros profissionais de saúde, materiais hospitalares, exames subsidiários, equipamentos diversos e remuneração dos Centros de Pesquisa.
III. A condução de um estudo envolvendo seres humanos prevê o envio de relatórios semestrais ao CEP de acordo com a Resolução 196/96 CNS/MS.
Assinale
I. A CONEP terá composição multi e transdisciplinar, com pessoas de ambos os sexos e deverá ser composta por 15 (quinze) membros titulares e seus respectivos suplentes.
II. Um dos documentos exigidos pela RDC 39/08 da ANVISA prevê o orçamento para a pesquisa. Este deve ser apresentado de forma detalhada prevendo recursos e especificando gastos com visitas médicas e de outros profissionais de saúde, materiais hospitalares, exames subsidiários, equipamentos diversos e remuneração dos Centros de Pesquisa.
III. A condução de um estudo envolvendo seres humanos prevê o envio de relatórios semestrais ao CEP de acordo com a Resolução 196/96 CNS/MS.
Assinale
Provas
Questão presente nas seguintes provas
- Farmacovigilância e EpidemiologiaFarmacovigilância
- LegislaçãoLegislação Federal, Normas e Resoluções do CFF
A RDC 04/2009 prevê, no capítulo 7, do artigo 13 ao 16, inspeções em farmacovigiância. Os detentores de registro de medicamentos (DRM) serão submetidos à inspeção em farmacovigilância pelo Sistema Nacional de Vigilância Sanitária (SNVS) sempre que houver necessidade de avaliação do cumprimento dessa Resolução. Além disso, as inspeções em farmacovigilância terão como objetivo a avaliação dos sistemas de farmacovigilância das empresas farmacêuticas. Sobre a inspeção em farmacovigilância para detentores de registro de medicamentos não é correto afirmar que:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container