Foram encontradas 900 questões.
Disciplina: TI - Redes de Computadores
Banca: CESPE / CEBRASPE
Orgão: UDESC
O protocolo WPA2 possui diversas características técnicas que o diferem de seus antecessores. Considerando as características de segurança no WPA2, julgue os itens subsequente.
O WPA2 requer o uso de criptografia simétrica com o algoritmo AES.
Provas
Disciplina: TI - Redes de Computadores
Banca: CESPE / CEBRASPE
Orgão: UDESC
O protocolo WPA2 possui diversas características técnicas que o diferem de seus antecessores. Considerando as características de segurança no WPA2, julgue os itens subsequente.
O WPA2 requer um protocolo de apresentação de duas vias que executa a autenticação individual de cada entidade sem derivação de chaves.
Provas
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
A matriz D (feedthrough direto) deve ser diferente de zero para representar corretamente o sistema considerado.
Provas
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
O sistema descrito tem ganho infinito para entrada em degrau em malha aberta.
Provas
Disciplina: Engenharia de Telecomunicações
Banca: CESPE / CEBRASPE
Orgão: UDESC
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
Se a frequência fs for menor que o dobro da maior frequência presente no sinal de saída do sistema, poderá ocorrer aliasing, causando distorções irreversíveis na reconstrução do sinal.
Provas
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
Para aplicar o critério de Nyquist à função de transferência em malha aberta, basta verificar se o diagrama envolve o ponto crítico (−1,0).
Provas
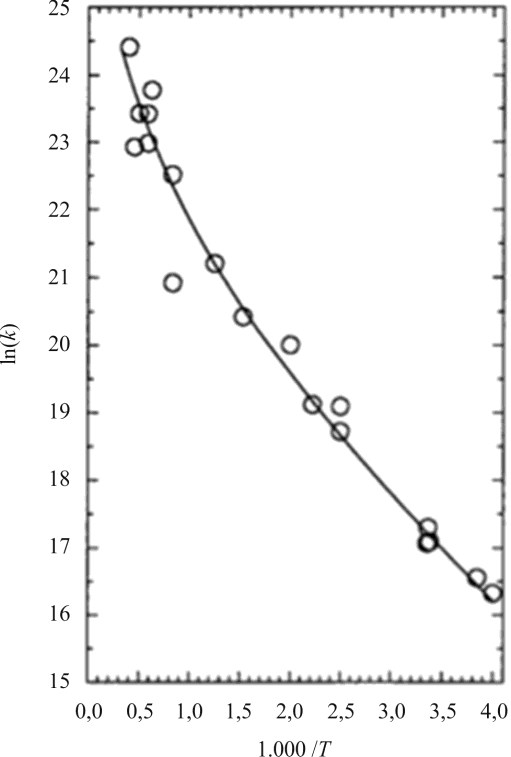
J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Nos resultados experimentais apresentados no gráfico, a constante de velocidade k obedece à lei usual de Arrhenius em toda a faixa de temperaturas do experimento.
Provas

J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Pela teoria usual de Arrhenius, a energia de ativação de uma reação química é constante, mas, segundo a teoria de Aquilanti-Mundim, ela varia com a temperatura.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
O valor do potencial-padrão da célula eletroquímica em questão é menor que 0,3 V.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
A variação da energia livre de Gibbs-padrão (\( \Delta Gº \)) para a reação em apreço é negativa, com valor inferior a −45 kJ/mol, o que indica que a reação é espontânea nas condições-padrão.
Provas
Caderno Container